Tỉ lệ mol là một khái niệm quan trọng trong hóa học, đặc biệt trong các bài toán liên quan đến phản ứng hóa học. Nó cho biết mối quan hệ về số lượng giữa các chất tham gia và sản phẩm trong một phản ứng.
Trong bài toán sau, chúng ta sẽ xem xét cách sử dụng tỉ lệ mol để giải quyết một bài toán cụ thể:
Cho hỗn hợp gồm Na và Al có tỉ lệ mol tương ứng là 1 : 2 vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là bao nhiêu?
Để giải quyết bài toán này, chúng ta cần hiểu rõ các phản ứng xảy ra và tỉ lệ mol giữa các chất.
Phản ứng đầu tiên là giữa Na và nước:
2Na + 2H2O → 2NaOH + H2
Phản ứng thứ hai là giữa Al và dung dịch NaOH tạo thành từ phản ứng trên:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Sau khi các phản ứng xảy ra hoàn toàn, chất rắn không tan còn lại là Al dư. Để tính được khối lượng Al dư, chúng ta cần xác định số mol của Na và Al ban đầu, sau đó tính toán lượng Al đã phản ứng và lượng Al còn dư.
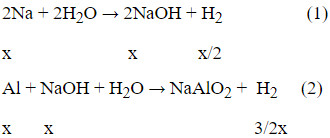 Sơ đồ phản ứng giữa Na, Al và nước, tạo thành NaOH và khí H2
Sơ đồ phản ứng giữa Na, Al và nước, tạo thành NaOH và khí H2
Số mol H2 thu được là 8,96 lít / 22,4 lít/mol = 0,4 mol.
Gọi số mol Na là x, thì số mol Al là 2x.
Từ phản ứng của Na và nước, ta có số mol NaOH tạo thành là x.
Từ phản ứng của Al và NaOH, ta có:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x mol NaOH sẽ phản ứng với x mol Al. Do đó, số mol Al dư là 2x – x = x.
Tổng số mol H2 tạo thành từ hai phản ứng là:
Từ phản ứng của Na: x/2 mol H2
Từ phản ứng của Al: (3/2)x mol H2
Vậy tổng số mol H2 là x/2 + (3/2)x = 2x = 0,4 mol. Suy ra x = 0,2 mol.
Số mol Al dư là x = 0,2 mol.
Khối lượng Al dư là m = 0,2 mol * 27 g/mol = 5,4 g.
Vậy giá trị của m là 5,4 gam.
Tóm lại, Tỉ Lệ Mol Là Gì?
Tỉ lệ mol là tỉ lệ giữa số mol của các chất trong một phản ứng hóa học. Nó giúp chúng ta xác định lượng chất cần thiết để phản ứng hoặc lượng sản phẩm tạo thành. Việc hiểu và áp dụng tỉ lệ mol là rất quan trọng để giải quyết các bài toán hóa học một cách chính xác. Trong ví dụ trên, việc xác định tỉ lệ mol giữa Na, Al và H2 đã giúp chúng ta tìm ra lượng Al dư sau phản ứng.
