Thuyết Vb (Valence Bond) và thuyết MO (Molecular Orbital) là hai phương pháp tiếp cận chính trong việc mô tả liên kết hóa học. Cả hai đều có những đóng góp quan trọng trong việc giải thích cấu trúc và tính chất của phân tử.
1. Điểm Giống Nhau Giữa Thuyết VB và Thuyết MO
Cả thuyết VB và thuyết MO đều đưa ra một số kết luận tương đồng về liên kết hóa học:
- Phân bố electron: Cả hai thuyết đều dự đoán sự phân bố electron tương tự trong phân tử.
- Sự tập trung mật độ electron: Yếu tố then chốt để hình thành liên kết cộng hóa trị là sự tập trung mật độ electron giữa hai hạt nhân nguyên tử.
- Sự che phủ của AO: Để hình thành liên kết, các orbital nguyên tử (AO) của các nguyên tử liên kết phải che phủ lên nhau.
- Phân loại liên kết: Cả hai thuyết đều phân biệt rõ ràng giữa liên kết sigma (σ) và liên kết pi (π).
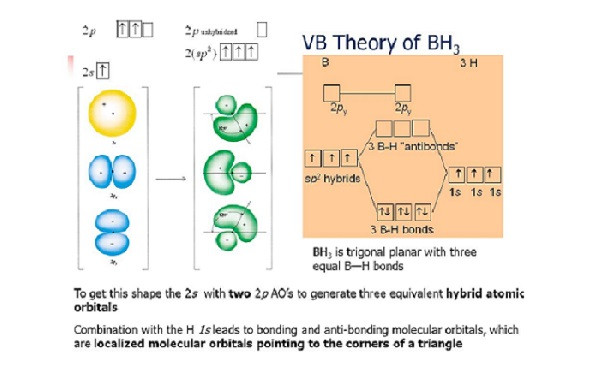 Sơ đồ so sánh thuyết VB và MO về sự hình thành liên kết cộng hóa trị, thể hiện sự che phủ của orbital nguyên tử và sự phân bố electron giữa các hạt nhân.
Sơ đồ so sánh thuyết VB và MO về sự hình thành liên kết cộng hóa trị, thể hiện sự che phủ của orbital nguyên tử và sự phân bố electron giữa các hạt nhân.
Sự tương đồng này thể hiện rõ nhất ở liên kết hai tâm. Thuyết VB, khác với thuyết MO, không thể xét đến liên kết nhiều tâm.
2. Điểm Khác Biệt Giữa Thuyết VB và Thuyết MO
Tuy có những điểm chung, thuyết VB và thuyết MO vẫn có những khác biệt đáng kể:
2.1. Thuyết VB (Valence Bond)
Thuyết VB tập trung vào việc mô tả sự hình thành liên kết bằng cách ghép đôi các electron hóa trị giữa các nguyên tử.
- Ưu điểm:
- Mô tả phân tử một cách trực quan, gần gũi với khái niệm hóa trị quen thuộc.
- Cho phép biểu diễn phân tử bằng công thức cấu tạo, thuận tiện trong việc trình bày lý thuyết.
2.2. Thuyết MO (Molecular Orbital)
Thuyết MO tiếp cận bằng cách kết hợp các orbital nguyên tử để tạo thành các orbital phân tử, trong đó electron có thể di chuyển tự do trên toàn phân tử.
- Ưu điểm:
- Tính nhất quán cao, cho phép mô tả liên kết hóa học trong bất kỳ phân tử nào, kể cả kim loại.
- Mô tả được trạng thái kích thích của phân tử, giải thích quang phổ electron của phân tử.
3. Kết Luận
Cả thuyết VB và thuyết MO đều là những công cụ hữu ích để hiểu về liên kết hóa học. Tuy nhiên, cần lưu ý rằng ngay cả khi sử dụng những kết quả chính xác nhất từ phương trình sóng Schrodinger, thuyết MO cũng chỉ mô tả trạng thái electron trong phân tử gần với trạng thái thực. Do đó, mọi kết luận rút ra từ thuyết VB hay MO chỉ được coi là xác thực khi phù hợp với kết quả thực nghiệm. Việc lựa chọn thuyết nào để sử dụng phụ thuộc vào bài toán cụ thể và mục đích nghiên cứu.
