Magie sulfat (MgSO4), còn được gọi là muối Epsom, là một hợp chất hóa học quan trọng với nhiều ứng dụng trong nông nghiệp, y học và công nghiệp. Để hiểu rõ về tính chất hóa học và khả năng tham gia phản ứng của MgSO4, việc xác định số oxi hóa của các nguyên tố trong hợp chất này là rất cần thiết.
Trong hợp chất MgSO4, ta có thể xác định số oxi hóa của từng nguyên tố như sau:
- Magie (Mg): Magie là kim loại thuộc nhóm IIA, do đó nó luôn có số oxi hóa là +2.
- Lưu huỳnh (S): Trong ion sulfat (SO4^2-), tổng số oxi hóa của oxi là -8 (4 nguyên tử oxi, mỗi nguyên tử có số oxi hóa -2). Vì ion sulfat có điện tích -2, số oxi hóa của lưu huỳnh phải là +6 để tổng số oxi hóa của ion sulfat bằng -2 (+6 + (-8) = -2).
- Oxi (O): Oxi thường có số oxi hóa là -2. Trong sulfat (SO4^2-), mỗi nguyên tử oxi có số oxi hóa là -2.
Như vậy, số oxi hóa của các nguyên tố trong MgSO4 là: Mg (+2), S (+6), và O (-2).
Phản ứng mà MgSO4 tham gia được đề cập trong bài viết gốc là một ví dụ về phản ứng oxi hóa khử:
Mg + H2SO4 → MgSO4 + H2S + H2O
Trong phản ứng này, magie (Mg) bị oxi hóa từ số oxi hóa 0 lên +2 (trong MgSO4), trong khi lưu huỳnh (S) trong H2SO4 bị khử một phần từ +6 xuống -2 (trong H2S).
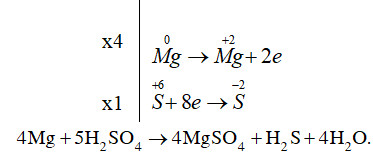 Phản ứng giữa magie và axit sunfuric tạo ra magie sulfat, hydro sunfua và nước
Phản ứng giữa magie và axit sunfuric tạo ra magie sulfat, hydro sunfua và nước
Cân bằng phương trình phản ứng oxi hóa khử:
Để cân bằng phương trình phản ứng, chúng ta cần xác định chất oxi hóa và chất khử, sau đó áp dụng phương pháp thăng bằng electron hoặc phương pháp ion-electron.
-
Xác định số oxi hóa:
- Mg: 0 → +2 (tăng 2)
- S trong H2SO4: +6 → -2 (trong H2S) (giảm 8)
-
Viết quá trình oxi hóa và khử:
- Oxi hóa: Mg → Mg^2+ + 2e
- Khử: S^+6 + 8e → S^-2
-
Cân bằng số electron: Để số electron cho bằng số electron nhận, ta nhân quá trình oxi hóa với 4.
- 4Mg → 4Mg^2+ + 8e
- S^+6 + 8e → S^-2
-
Viết phương trình cân bằng:
4Mg + 5H2SO4 → 4MgSO4 + H2S + 4H2O
Trong phương trình cân bằng này, hệ số của H2O là 4, đúng như đáp án trong bài viết gốc.
Ứng dụng của MgSO4:
MgSO4 có nhiều ứng dụng quan trọng:
- Nông nghiệp: Là nguồn cung cấp magie và lưu huỳnh cho cây trồng, giúp tăng năng suất và chất lượng nông sản.
- Y học: Được sử dụng làm thuốc nhuận tràng, thuốc giãn cơ, và thuốc chống co giật.
- Công nghiệp: Được sử dụng trong sản xuất giấy, dệt may, và chất tẩy rửa.
Hiểu rõ số oxi hóa của các nguyên tố trong MgSO4 và các phản ứng mà nó tham gia giúp chúng ta ứng dụng hiệu quả hợp chất này trong nhiều lĩnh vực khác nhau.