Khái Niệm Phenol
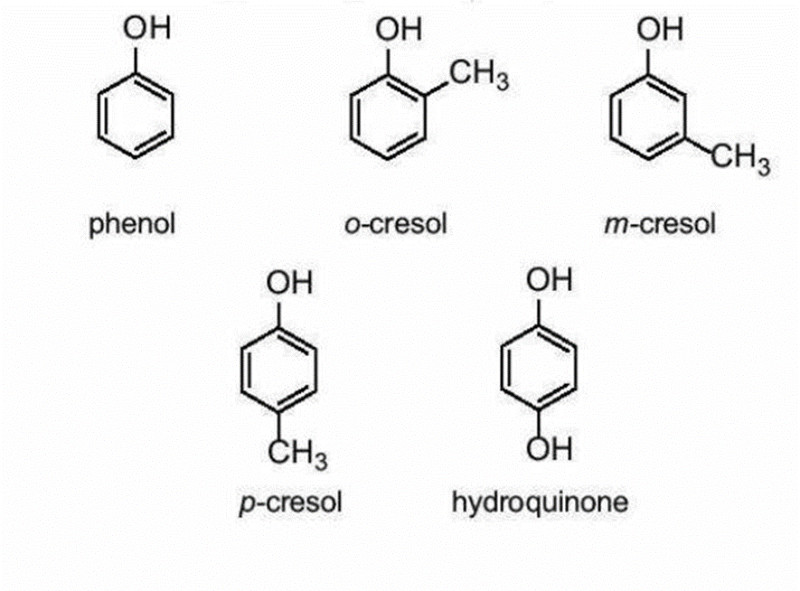
Phenol Là Hợp Chất Hữu Cơ Mà phân tử của nó chứa nhóm hydroxyl (-OH) liên kết trực tiếp với một nguyên tử carbon của vòng benzene. Công thức hóa học đơn giản nhất của phenol là C6H5OH. Phenol và các dẫn xuất của nó đóng vai trò quan trọng trong nhiều lĩnh vực công nghiệp và đời sống.
Hình ảnh minh họa công thức cấu tạo của phenol, cresol và các đồng phân của nó, thể hiện rõ nhóm -OH liên kết trực tiếp với vòng benzene.
Cấu Tạo Phân Tử và Phân Loại
Do ảnh hưởng của vòng benzene, liên kết O-H trong phenol phân cực mạnh hơn so với alcohol thông thường, làm cho phenol có tính acid yếu.
Hình ảnh thể hiện sự phân cực của liên kết O-H trong phân tử phenol, giải thích tính acid yếu của phenol so với alcohol.
Dựa trên số lượng nhóm -OH trong phân tử, phenol được chia thành:
- Monophenol: Chứa một nhóm -OH.
Hình ảnh minh họa công thức cấu tạo của phenol, một monophenol điển hình với một nhóm hydroxyl gắn vào vòng benzene.
- Polyphenol: Chứa nhiều nhóm -OH.
Hình ảnh công thức cấu tạo của Resorcinol, một polyphenol với hai nhóm hydroxyl liên kết trực tiếp với vòng benzene.
Tính Chất Vật Lý
- Phenol là chất rắn không màu ở điều kiện thường, nóng chảy ở 43°C.
- Nhiệt độ sôi và nhiệt độ nóng chảy cao hơn aryl halide tương đương do khả năng tạo liên kết hydrogen.
- Ít tan trong nước lạnh, tan vô hạn ở 66°C và tan tốt trong dung môi hữu cơ.
- Dễ bị chảy rữa, độc hại và gây bỏng.
Hình ảnh mô tả liên kết hydrogen giữa các phân tử phenol (a) và giữa phenol và phân tử nước (b), giải thích khả năng hòa tan và nhiệt độ sôi cao của phenol.
Tính Chất Hóa Học
Do ảnh hưởng qua lại giữa nhóm -OH và vòng benzene, phenol có thể tham gia phản ứng thế H ở nhóm -OH (tính acid) và thế H trên vòng benzene.
Hình ảnh tóm tắt các phản ứng hóa học quan trọng của phenol, bao gồm tính acid và phản ứng thế trên vòng benzene.
Tính acid:
- Phenol có tính acid yếu, không làm đổi màu quỳ tím.
- Phản ứng với NaOH: C6H5OH + NaOH → C6H5ONa + H2O
- Phản ứng với Na2CO3: C6H5OH + Na2CO3 ⇌ C6H5ONa + NaHCO3
Hình ảnh minh họa phản ứng giữa phenol và NaOH, tạo thành muối phenolat và nước, thể hiện tính acid của phenol.
Phản ứng thế trên vòng benzene:
- Phản ứng với nước bromine tạo kết tủa trắng:
Hình ảnh phản ứng của phenol với nước bromine, tạo thành kết tủa trắng 2,4,6-tribromophenol, một phản ứng đặc trưng để nhận biết phenol.
- Phản ứng với HNO3 đặc tạo 2,4,6-trinitrophenol (axit picric):
Hình ảnh phản ứng của phenol với axit nitric đặc, tạo thành axit picric (2,4,6-trinitrophenol), một chất nổ mạnh.
Ứng Dụng và Điều Chế
Ứng dụng:
Hình ảnh tổng hợp các ứng dụng đa dạng của phenol, từ sản xuất nhựa, dược phẩm, chất khử trùng đến thuốc trừ sâu.
- Sản xuất nhựa epoxy và nhựa phenol-formaldehyde.
- Sản xuất phẩm nhuộm, thuốc nổ, chất diệt nấm mốc, chất diệt cỏ.
- Chất khử trùng, tẩy uế.
Điều chế:
- Tách từ nhựa than đá.
- Sản xuất từ cumene: