Este là một hợp chất hữu cơ quan trọng, có nhiều ứng dụng trong đời sống và công nghiệp. Một trong những đặc điểm quan trọng của este là nhiệt độ sôi. Vậy, phát biểu nào sau đây là sai khi so sánh nhiệt độ sôi của este với ancol có cùng phân tử khối? Để trả lời câu hỏi này, chúng ta cùng tìm hiểu chi tiết về este và các yếu tố ảnh hưởng đến nhiệt độ sôi của chúng.
1. Este là gì?
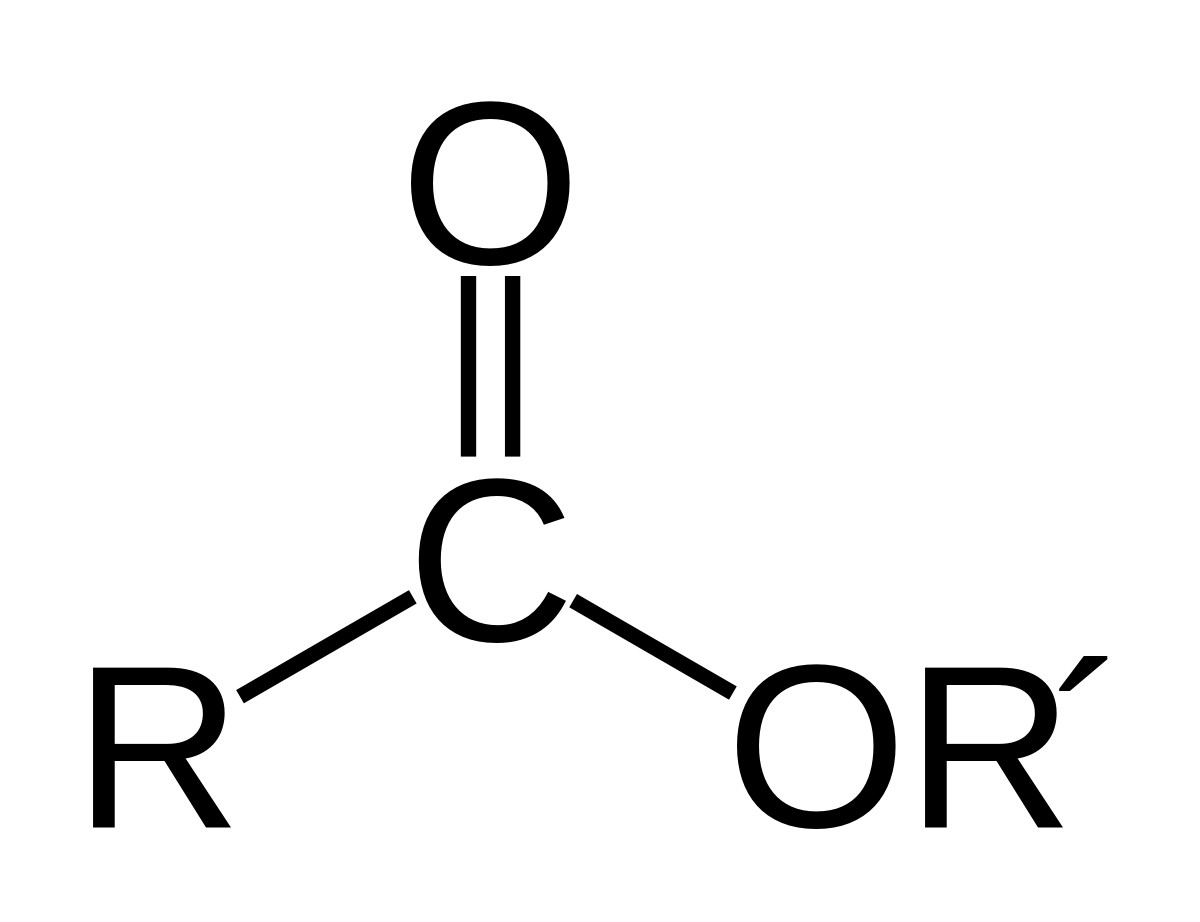
Este là sản phẩm của phản ứng giữa axit cacboxylic và ancol, trong đó nhóm OH của axit được thay thế bằng nhóm OR’ (R’ là gốc hidrocacbon). Công thức chung của este đơn chức là RCOOR’.
Alt: Cấu tạo phân tử este đơn chức, công thức RCOOR’
2. Tính chất vật lý của este
- Trạng thái: Đa số este ở trạng thái lỏng ở điều kiện thường. Các este có khối lượng phân tử lớn có thể tồn tại ở trạng thái rắn (ví dụ: sáp ong).
- Độ tan: Este thường ít tan trong nước do không tạo được liên kết hydro với nước.
- Mùi: Nhiều este có mùi thơm đặc trưng, được ứng dụng trong công nghiệp thực phẩm và mỹ phẩm. Ví dụ, isoamyl axetat có mùi chuối, etyl butirat có mùi dứa.
- Nhiệt độ sôi: Este có nhiệt độ sôi thấp hơn so với ancol và axit cacboxylic có cùng phân tử khối. Đây là một trong những tính chất quan trọng nhất để phân biệt este với các hợp chất hữu cơ khác.
3. Tại sao nhiệt độ sôi của este lại thấp hơn ancol?
Nguyên nhân chính khiến nhiệt độ sôi của este thấp hơn ancol là do khả năng tạo liên kết hydro.
- Ancol: Các phân tử ancol (R-OH) có khả năng tạo liên kết hydro mạnh mẽ giữa các phân tử với nhau thông qua nhóm -OH. Liên kết hydro là một lực hút tương đối mạnh, đòi hỏi nhiều năng lượng hơn để phá vỡ, dẫn đến nhiệt độ sôi cao.
- Este: Các phân tử este (R-COO-R’) có liên kết C=O phân cực nhưng không có liên kết O-H. Điều này khiến este không thể tạo liên kết hydro giữa các phân tử este với nhau. Lực tương tác giữa các phân tử este chủ yếu là lực Van der Waals yếu hơn nhiều so với liên kết hydro.
Alt: So sánh liên kết hydro giữa ancol và este
4. Các yếu tố ảnh hưởng đến nhiệt độ sôi của este
Ngoài khả năng tạo liên kết hydro, một số yếu tố khác cũng ảnh hưởng đến nhiệt độ sôi của este:
- Khối lượng phân tử: Este có khối lượng phân tử càng lớn thì nhiệt độ sôi càng cao do lực Van der Waals tăng lên.
- Cấu trúc mạch: Este mạch thẳng thường có nhiệt độ sôi cao hơn este mạch nhánh do diện tích bề mặt tiếp xúc lớn hơn, dẫn đến lực Van der Waals mạnh hơn.
- Độ phân cực: Este có độ phân cực cao hơn thường có nhiệt độ sôi cao hơn do lực hút tĩnh điện giữa các phân tử mạnh hơn.
5. Ứng dụng thực tế của nhiệt độ sôi thấp của este
Nhiệt độ sôi thấp của este mang lại nhiều ứng dụng quan trọng:
- Dung môi: Este được sử dụng làm dung môi trong nhiều ngành công nghiệp do dễ bay hơi và hòa tan được nhiều chất hữu cơ.
- Hương liệu: Nhiều este có mùi thơm đặc trưng, được sử dụng làm hương liệu trong công nghiệp thực phẩm và mỹ phẩm. Việc dễ bay hơi giúp lan tỏa hương thơm.
- Sản xuất polyme: Một số este là monome để sản xuất polyme. Nhiệt độ sôi thấp giúp dễ dàng tách monome khỏi sản phẩm.
Alt: Ứng dụng của este trong công nghiệp mỹ phẩm
6. Kết luận
Như vậy, phát biểu “Nhiệt độ sôi của este thấp hơn hẳn so với ancol có cùng phân tử khối” là một phát biểu đúng. Điều này được giải thích bởi sự khác biệt trong khả năng tạo liên kết hydro giữa các phân tử este và ancol. Ancol tạo được liên kết hydro mạnh mẽ, trong khi este thì không, dẫn đến nhiệt độ sôi thấp hơn. Hiểu rõ tính chất này giúp chúng ta ứng dụng este một cách hiệu quả trong nhiều lĩnh vực của đời sống và công nghiệp.