Phân tử khối là một khái niệm quan trọng trong hóa học, đặc biệt khi nghiên cứu về các nguyên tố và hợp chất. Trong bài viết này, chúng ta sẽ đi sâu vào phân tử khối của chì (Pb), cách xác định nó và những ứng dụng liên quan.
Chì (Pb) là một nguyên tố hóa học có số nguyên tử 82, nằm trong nhóm 14 của bảng tuần hoàn. Chì là một kim loại nặng, mềm, dễ uốn và có màu xám xanh. Do có nhiều đồng vị khác nhau, việc xác định Phân Tử Khối Pb cần được thực hiện một cách cẩn thận.
Định Nghĩa Phân Tử Khối Pb
Phân tử khối của chì (Pb), hay còn gọi là nguyên tử khối trung bình của chì, là giá trị trung bình cộng của khối lượng các đồng vị của chì, có xét đến tỷ lệ phần trăm của từng đồng vị trong tự nhiên.
Công thức tính phân tử khối Pb:
Phân tử khối Pb = ( (% đồng vị 1 * khối lượng đồng vị 1) + (% đồng vị 2 * khối lượng đồng vị 2) + ... ) / 100Trong đó:
- % đồng vị: Tỷ lệ phần trăm của đồng vị đó trong tự nhiên.
- Khối lượng đồng vị: Khối lượng của một nguyên tử của đồng vị đó (đơn vị amu).
Các Đồng Vị Của Chì (Pb) và Cách Tính Phân Tử Khối
Chì có 4 đồng vị bền trong tự nhiên, đó là Pb-204, Pb-206, Pb-207 và Pb-208. Mỗi đồng vị này có khối lượng và tỷ lệ phần trăm khác nhau, ảnh hưởng đến phân tử khối trung bình của chì.
Alt text: Bảng thống kê thành phần các đồng vị của chì (Pb) bao gồm Pb-204, Pb-206, Pb-207, và Pb-208, thể hiện phần trăm tồn tại trong tự nhiên và nguyên tử khối tương ứng, dùng để tính nguyên tử khối trung bình.
Để tính phân tử khối Pb, ta cần biết tỷ lệ phần trăm và khối lượng của từng đồng vị. Ví dụ, nếu chúng ta có thông tin sau:
- Pb-204: 1.4%
- Pb-206: 24.1%
- Pb-207: 22.1%
- Pb-208: 52.4%
Khi đó, phân tử khối Pb sẽ được tính như sau:
Phân tử khối Pb = ( (1.4 * 204) + (24.1 * 206) + (22.1 * 207) + (52.4 * 208) ) / 100Phân tử khối Pb ≈ 207.2Vậy, phân tử khối của chì xấp xỉ bằng 207.2 amu.
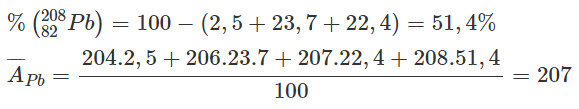 Cách giải chi tiết bài tập tính nguyên tử khối trung bình của chì (Pb) trong sách bài tập Hóa học 10
Cách giải chi tiết bài tập tính nguyên tử khối trung bình của chì (Pb) trong sách bài tập Hóa học 10
Alt text: Hướng dẫn giải bài tập hóa học lớp 10 về cách tính nguyên tử khối trung bình của chì (Pb), trình bày chi tiết các bước áp dụng công thức và thay số liệu của các đồng vị chì.
Ứng Dụng Của Việc Xác Định Phân Tử Khối Pb
Việc xác định chính xác phân tử khối Pb có nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau:
- Nghiên cứu khoa học: Phân tử khối Pb chính xác là cơ sở để thực hiện các nghiên cứu về tính chất hóa học và vật lý của chì và các hợp chất của nó.
- Công nghiệp: Trong sản xuất và chế tạo các sản phẩm chứa chì, việc biết phân tử khối giúp kiểm soát chất lượng và tính toán tỷ lệ thành phần chính xác.
- Địa chất học: Các nhà địa chất sử dụng tỷ lệ đồng vị của chì để xác định tuổi của các mẫu khoáng vật và đá, từ đó nghiên cứu về lịch sử hình thành trái đất.
- Môi trường: Phân tích tỷ lệ đồng vị chì trong các mẫu môi trường (đất, nước, không khí) giúp xác định nguồn gốc và mức độ ô nhiễm chì, từ đó đưa ra các biện pháp xử lý phù hợp.
Lưu Ý Về Độ Chính Xác
Độ chính xác của phân tử khối Pb phụ thuộc vào độ chính xác của các phép đo tỷ lệ đồng vị và khối lượng đồng vị. Các phương pháp đo phổ khối lượng hiện đại cho phép xác định các giá trị này với độ chính xác rất cao, giúp tính toán phân tử khối Pb một cách chính xác nhất.
Kết Luận
Phân tử khối Pb là một thông số quan trọng, được xác định dựa trên tỷ lệ các đồng vị của chì trong tự nhiên. Việc hiểu rõ cách tính và ứng dụng của phân tử khối Pb có ý nghĩa quan trọng trong nhiều lĩnh vực khoa học và công nghiệp. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích về chủ đề này.
