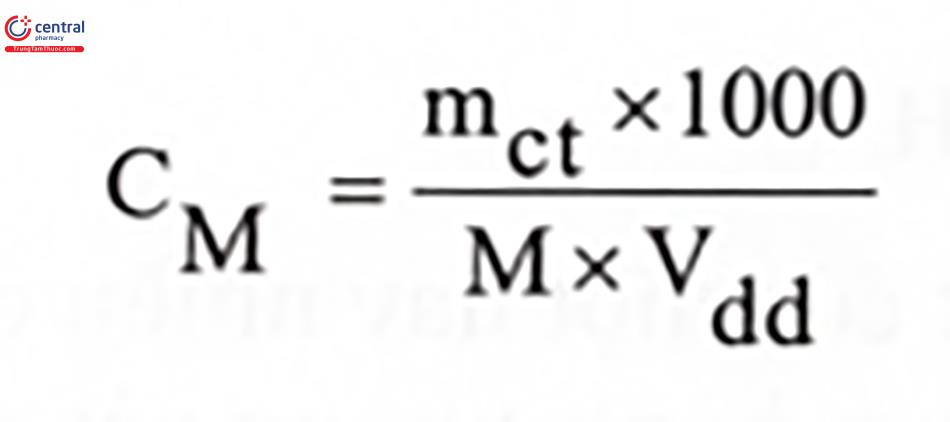Trong lĩnh vực xét nghiệm y học và nghiên cứu khoa học, việc hiểu rõ và sử dụng chính xác các đơn vị đo lường nồng độ dung dịch là vô cùng quan trọng. Bài viết này sẽ tập trung vào một khái niệm quan trọng: Nồng độ đương Lượng Gam, đồng thời cung cấp thông tin chi tiết về cách tính toán và ứng dụng của nó.
Các Loại Nồng Độ Dung Dịch Thường Gặp
Trước khi đi sâu vào nồng độ đương lượng gam, chúng ta hãy điểm qua một số loại nồng độ dung dịch phổ biến khác:
- Nồng độ phần trăm (C%): Biểu thị lượng chất tan trong 100 đơn vị dung dịch. Có nhiều dạng như khối lượng/khối lượng, khối lượng/thể tích và thể tích/thể tích.
- Nồng độ mol/lít (M): Số mol chất tan trong 1 lít dung dịch.
M) trong đó các biến được giải thích.* - Nồng độ đương lượng (CN): Số đương lượng gam chất tan trong 1 lít dung dịch. Đây là trọng tâm của bài viết này.
Nồng Độ Đương Lượng Gam (CN) Là Gì?
Định nghĩa: Nồng độ đương lượng gam (CN) biểu thị số đương lượng gam của chất tan có trong một lít dung dịch. Đây là một cách biểu thị nồng độ dựa trên khả năng phản ứng của chất tan, đặc biệt hữu ích trong các phản ứng hóa học, đặc biệt là phản ứng trung hòa và oxy hóa khử.
Công thức:
alt: Phương trình toán học biểu diễn cách tính nồng độ đương lượng, với ký hiệu và biến số được giải thích đầy đủ.
Trong đó:
- mct: Khối lượng chất tan (g)
- Vdd: Thể tích dung dịch (L)
- E: Đương lượng gam của chất tan
Vậy, Đương Lượng Gam (E) Là Gì?
Đương lượng gam của một chất là khối lượng của chất đó, tính bằng gam, có khả năng phản ứng vừa đủ với một đương lượng gam hydro (H+) hoặc một đương lượng gam của một chất bất kỳ khác. Đương lượng gam phụ thuộc vào loại phản ứng mà chất đó tham gia.
Công thức tính đương lượng gam:
E = M / n
Trong đó:
-
M: Phân tử gam của chất
-
n: Số đương lượng, có thể là:
- Số ion H+ mà một phân tử axit cho trong phản ứng.
- Số ion H+ mà một phân tử bazơ nhận trong phản ứng.
- Tổng điện tích của ion kim loại (cation) trong một phân tử muối tham gia phản ứng.
- Số electron mà một phân tử chất oxy hóa hoặc chất khử trao đổi trong phản ứng oxy hóa khử.
Ví dụ minh họa:
Xét phản ứng trung hòa giữa axit sulfuric (H2SO4) và natri hydroxit (NaOH):
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Trong phản ứng này, một phân tử H2SO4 cho 2 ion H+. Do đó, n = 2.
Nếu phân tử gam của H2SO4 là 98 g/mol, thì đương lượng gam của H2SO4 trong phản ứng này là:
E = 98 g/mol / 2 = 49 g/đương lượng
Ứng Dụng Của Nồng Độ Đương Lượng Gam
Nồng độ đương lượng gam đặc biệt hữu ích trong các tình huống sau:
- Phản ứng trung hòa: Khi tính toán lượng axit và bazơ cần thiết để trung hòa lẫn nhau. Do một đương lượng gam axit sẽ phản ứng vừa đủ với một đương lượng gam bazơ.
- Phản ứng oxy hóa khử: Khi tính toán lượng chất oxy hóa và chất khử cần thiết trong một phản ứng.
- Chuẩn độ: Trong các thí nghiệm chuẩn độ, nồng độ đương lượng gam giúp xác định nồng độ của một dung dịch chưa biết bằng cách phản ứng nó với một dung dịch đã biết nồng độ.
Ví Dụ Về Pha Chế Dung Dịch Theo Nồng Độ Đương Lượng
Ví dụ: Pha 100 mL dung dịch 0,1 N muối bari clorua (BaCl2.2H2O).
- Khối lượng mol của BaCl2.2H2O là 244 g/mol. Vì bari có điện tích 2+, n = 2.
- Đương lượng gam của BaCl2.2H2O là 244 g/mol / 2 = 122 g/đương lượng.
- Dung dịch BaCl2.2H2O có nồng độ 0,1 N nghĩa là trong 1 lít dung dịch có 0,1 đương lượng gam, tương đương 12,2 g BaCl2.2H2O.
- Vậy, trong 100 mL dung dịch có 1,22 g BaCl2.2H2O.
- Tiến hành cân 1,22g BaCl2.2H2O hòa tan vào nước cất và định mức thành 100ml.
Lưu Ý Quan Trọng Khi Pha Chế Dung Dịch
- Sử dụng dụng cụ chính xác: Ống đong, bình định mức, pipet phải được hiệu chuẩn và sử dụng đúng cách.
- Nước cất: Luôn sử dụng nước cất hoặc nước khử ion để pha chế dung dịch.
- Tính toán cẩn thận: Đảm bảo tính toán chính xác lượng chất tan và dung môi cần thiết.
- Kiểm tra lại: Nếu có thể, kiểm tra lại nồng độ dung dịch sau khi pha chế bằng các phương pháp phù hợp.
Kết Luận
Nồng độ đương lượng gam là một khái niệm quan trọng trong hóa học và các ngành khoa học liên quan. Việc nắm vững định nghĩa, cách tính toán và ứng dụng của nó sẽ giúp bạn thực hiện các thí nghiệm và xét nghiệm một cách chính xác và hiệu quả. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích và cần thiết về chủ đề này.