Nguyên tử là nền tảng của mọi vật chất trong vũ trụ. Hiểu rõ về cấu tạo nguyên tử là chìa khóa để khám phá thế giới hóa học và vật lý. Vậy, Nguyên Tử Cấu Tạo Gồm Mấy Phần? Bài viết này sẽ cung cấp thông tin chi tiết và dễ hiểu nhất về cấu trúc phức tạp này.
1. Thành Phần Cơ Bản Của Nguyên Tử
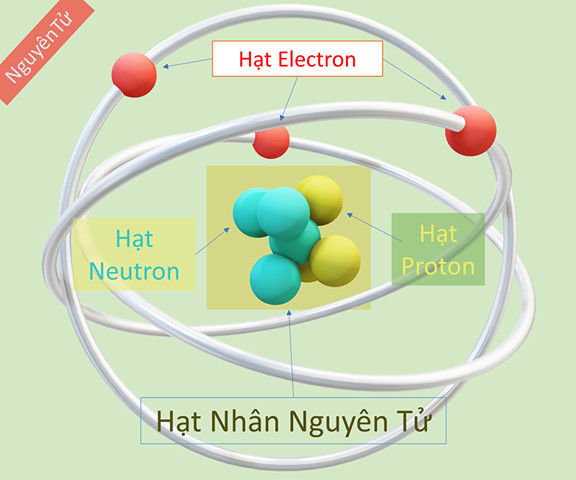
Nguyên tử không phải là một khối đặc mà được tạo thành từ các hạt nhỏ hơn nhiều. Cấu trúc của nó bao gồm hai phần chính:
- Hạt nhân: Nằm ở trung tâm nguyên tử, chứa các hạt proton mang điện tích dương và neutron không mang điện.
- Vỏ nguyên tử: Bao quanh hạt nhân, chứa các electron mang điện tích âm.
Hình ảnh mô tả cấu tạo nguyên tử với hạt nhân chứa proton và neutron, cùng vỏ nguyên tử chứa các electron chuyển động xung quanh.
1.1. Hạt Nhân Nguyên Tử
Hạt nhân là trung tâm điều khiển của nguyên tử, quyết định phần lớn khối lượng của nguyên tử.
- Proton (p): Mang điện tích dương (+1), số lượng proton trong hạt nhân xác định nguyên tố hóa học của nguyên tử. Ví dụ, tất cả các nguyên tử có 1 proton đều là nguyên tử hydro.
- Neutron (n): Không mang điện tích (trung hòa), có khối lượng gần bằng proton. Số lượng neutron có thể khác nhau ở các nguyên tử của cùng một nguyên tố, tạo ra các đồng vị.
1.2. Vỏ Nguyên Tử
Vỏ nguyên tử là không gian xung quanh hạt nhân, nơi các electron chuyển động.
- Electron (e): Mang điện tích âm (-1), có khối lượng rất nhỏ so với proton và neutron. Electron chuyển động xung quanh hạt nhân theo các quỹ đạo nhất định, tạo thành các lớp electron. Số lượng electron bằng với số lượng proton trong nguyên tử trung hòa về điện.
2. Các Lớp và Phân Lớp Electron
Electron không phân bố ngẫu nhiên trong vỏ nguyên tử mà được sắp xếp theo các lớp và phân lớp năng lượng khác nhau.
2.1. Lớp Electron
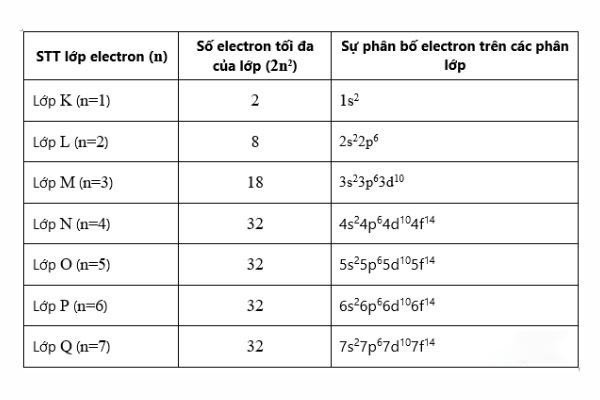
Các lớp electron được đánh số từ 1 đến 7 (hoặc ký hiệu bằng các chữ cái K, L, M, N, O, P, Q), bắt đầu từ lớp gần hạt nhân nhất. Mỗi lớp có một mức năng lượng nhất định và có thể chứa một số lượng electron tối đa.
| Mức năng lượng (n) | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|---|---|---|---|---|---|---|---|
| Tên lớp | K | L | M | N | O | P | Q |
| Số electron tối đa | 2 | 8 | 18 | 32 | 50 | 72 | 98 |
2.2. Phân Lớp Electron
Mỗi lớp electron lại được chia thành các phân lớp nhỏ hơn, gọi là phân lớp electron. Có bốn loại phân lớp chính: s, p, d, và f. Mỗi phân lớp có một hình dạng quỹ đạo đặc trưng và chứa một số lượng electron tối đa.
| Phân lớp | s | p | d | f |
|---|---|---|---|---|
| Số electron tối đa | 2 | 6 | 10 | 14 |
| Ký hiệu | s2 | p6 | d10 | f14 |
Bảng thống kê số electron tối đa trong mỗi lớp và phân lớp electron của nguyên tử.
3. Kích Thước và Khối Lượng Nguyên Tử
Nguyên tử có kích thước vô cùng nhỏ bé.
- Kích thước: Đường kính nguyên tử khoảng 10-10 m (1 Ångström), đường kính hạt nhân khoảng 10-14 m.
- Khối lượng: Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân. Đơn vị khối lượng nguyên tử là u (đvC), với 1 u ≈ 1.6605 x 10-27 kg.
4. Tổng Kết
Tóm lại, để trả lời cho câu hỏi nguyên tử cấu tạo gồm mấy phần, chúng ta có thể khẳng định: Nguyên tử được cấu tạo từ hai phần chính là hạt nhân (chứa proton và neutron) và vỏ nguyên tử (chứa electron). Sự sắp xếp và tương tác của các hạt này quyết định tính chất hóa học và vật lý của nguyên tố. Việc nắm vững kiến thức về cấu tạo nguyên tử là nền tảng quan trọng để hiểu sâu hơn về thế giới xung quanh ta.
