Liên Kết Kim Loại Là một khái niệm then chốt trong hóa học và khoa học vật liệu, đóng vai trò thiết yếu trong việc xác định các tính chất đặc trưng của kim loại. Hiểu rõ về liên kết kim loại giúp chúng ta nắm bắt được tại sao kim loại lại dẫn điện, dẫn nhiệt tốt, có độ dẻo cao và độ bền cơ học ấn tượng. Bài viết này sẽ đi sâu vào bản chất, cơ chế hình thành, đặc điểm, ứng dụng và tầm quan trọng của liên kết kim loại trong đời sống và công nghiệp.
1. Định Nghĩa Liên Kết Kim Loại
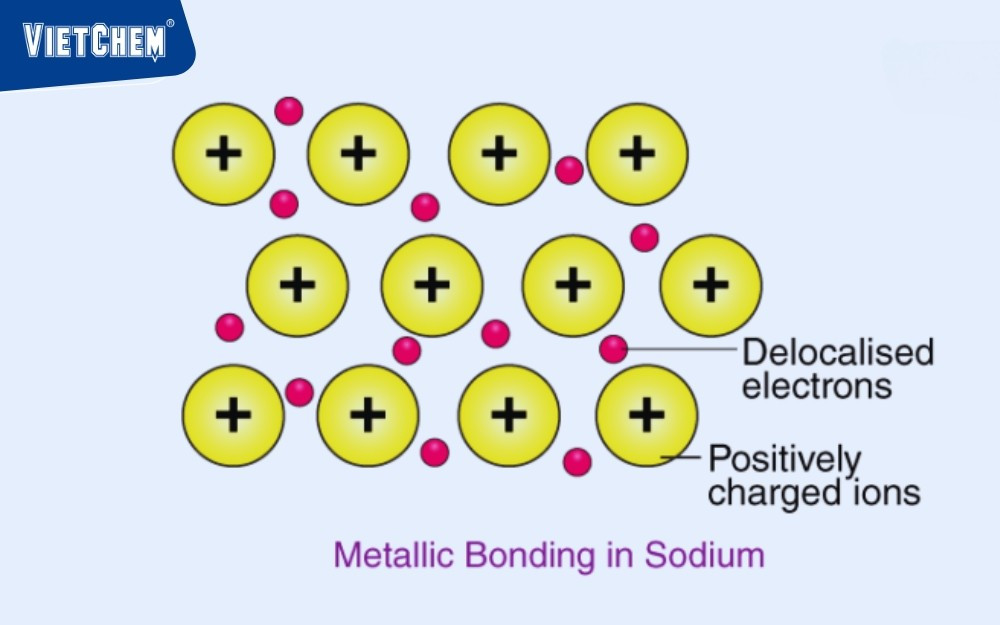
Liên kết kim loại là một loại liên kết hóa học hình thành giữa các nguyên tử kim loại. Điểm đặc biệt của liên kết này là sự tồn tại của một “biển electron” tự do, bao quanh và liên kết các ion kim loại dương (cation). Các electron này không thuộc về bất kỳ một nguyên tử cụ thể nào mà tự do di chuyển trong toàn bộ cấu trúc mạng tinh thể kim loại.
Giải Thích Chi Tiết:
- Khi các nguyên tử kim loại tập hợp lại, các electron hóa trị (electron lớp ngoài cùng) của chúng tách ra khỏi nguyên tử và trở thành electron tự do.
- “Biển electron” này đóng vai trò như một chất keo kết dính, liên kết các ion dương lại với nhau, tạo thành một cấu trúc mạng tinh thể kim loại ổn định và bền vững.
Ví dụ thực tế về liên kết kim loại: Trong các kim loại như đồng (Cu), sắt (Fe) hoặc nhôm (Al), liên kết kim loại là yếu tố chính quyết định khả năng dẫn điện, dẫn nhiệt và độ bền cao của chúng.
2. Các Đặc Điểm Nổi Bật Của Liên Kết Kim Loại
Liên kết kim loại mang lại cho kim loại những đặc tính độc đáo, khác biệt so với các loại vật liệu khác. Dưới đây là những đặc điểm quan trọng nhất:
2.1. Tính Dẫn Điện và Dẫn Nhiệt Vượt Trội:
- “Biển electron” tự do hoạt động như những hạt tải điện, dễ dàng di chuyển trong mạng tinh thể khi có điện trường hoặc gradient nhiệt độ, giúp truyền dẫn điện và nhiệt một cách hiệu quả.
- Ví dụ: Đồng (Cu) và bạc (Ag) là những kim loại dẫn điện tốt nhất, được sử dụng rộng rãi trong dây dẫn điện, mạch điện tử và các ứng dụng điện khác.
2.2. Tính Dẻo và Khả Năng Uốn, Dát Mỏng:
- Các ion kim loại có thể trượt qua nhau một cách dễ dàng mà không làm phá vỡ liên kết kim loại. Điều này cho phép kim loại có thể được uốn cong, kéo thành sợi hoặc dát mỏng mà không bị gãy vỡ.
- Ví dụ: Vàng (Au) có thể được dát mỏng thành lá vàng (gold leaf) để sử dụng trong trang trí và các ứng dụng khác nhờ tính dẻo cao.
2.3. Độ Bền Cơ Học Cao:
- Liên kết kim loại giúp kim loại có khả năng chịu được lực nén, lực kéo và va đập mạnh mà không bị biến dạng hoặc phá hủy cấu trúc.
- Ví dụ: Thép (hợp kim của sắt và carbon) được sử dụng rộng rãi trong xây dựng các tòa nhà cao tầng, cầu cống và các công trình cơ sở hạ tầng khác nhờ khả năng chịu lực tuyệt vời.
2.4. Độ Bóng Sáng:
- Các electron tự do trong “biển electron” có khả năng hấp thụ và phản xạ ánh sáng trên một dải tần rộng, tạo nên bề mặt sáng bóng đặc trưng của kim loại.
- Ví dụ: Bạc (Ag), nhôm (Al) và chrome (Cr) có độ bóng cao và được sử dụng rộng rãi trong trang trí, mạ và các ứng dụng khác.
3. Cơ Chế Hình Thành Liên Kết Kim Loại
Cơ chế hình thành liên kết kim loại có thể được giải thích thông qua cấu trúc mạng tinh thể và sự tham gia của electron tự do:
3.1. Quá Trình Hình Thành:
- Khi các nguyên tử kim loại sắp xếp trong cấu trúc mạng tinh thể, các electron hóa trị của chúng tách khỏi nguyên tử.
- Các electron này tạo thành một “biển electron” tự do, chuyển động hỗn loạn trong toàn bộ mạng tinh thể.
- Sự tương tác giữa “biển electron” tự do và các ion kim loại dương tạo ra một lực hút tĩnh điện mạnh mẽ, giữ các ion dương lại với nhau và tạo nên một cấu trúc bền vững.
3.2. Kết Quả:
- Sự tồn tại của “biển electron” không chỉ giúp kim loại liên kết chắc chắn mà còn mang lại khả năng dẫn điện, dẫn nhiệt và độ bền cơ học cao.
Ví dụ: Liên kết kim loại trong nhôm (Al) không chỉ giúp vật liệu này nhẹ mà còn đủ mạnh để sử dụng trong ngành hàng không vũ trụ.
4. Ứng Dụng Thực Tế Của Liên Kết Kim Loại
Liên kết kim loại là yếu tố then chốt tạo nên giá trị của kim loại trong đời sống hàng ngày và trong nhiều ngành công nghiệp khác nhau. Dưới đây là một số ứng dụng quan trọng:
4.1. Trong Xây Dựng:
- Kim loại như thép (Fe), nhôm (Al) được sử dụng rộng rãi nhờ độ bền cao và tính linh hoạt trong gia công.
- Thép chịu lực tốt, thích hợp để xây dựng cầu, khung nhà cao tầng và các công trình cơ sở hạ tầng khác.
- Nhôm nhẹ, chống ăn mòn, thích hợp để làm cửa sổ, vách ngăn và các chi tiết kiến trúc khác.
4.2. Trong Điện Tử:
- Đồng (Cu), bạc (Ag) được sử dụng làm dây dẫn điện trong các thiết bị điện tử do khả năng dẫn điện vượt trội.
- Nhôm (Al) được dùng trong sản xuất tản nhiệt và linh kiện điện tử nhờ tính dẫn nhiệt tốt.
4.3. Trong Sản Xuất và Giao Thông Vận Tải:
- Nhôm (Al) và hợp kim nhôm được sử dụng để chế tạo khung máy bay, thân tàu, vỏ ô tô nhờ trọng lượng nhẹ và khả năng chịu lực.
- Thép không gỉ được sử dụng trong ngành đóng tàu và sản xuất các thiết bị công nghiệp nặng nhờ khả năng chống ăn mòn và độ bền cao.
4.4. Trong Đời Sống Hàng Ngày:
- Các dụng cụ nhà bếp như nồi, chảo thường được làm từ nhôm hoặc thép không gỉ nhờ khả năng dẫn nhiệt tốt và độ bền cao.
- Đồ trang sức từ vàng (Au), bạc (Ag) không chỉ đẹp mà còn bền và dễ gia công nhờ tính dẻo.
5. Tầm Quan Trọng Của Liên Kết Kim Loại
Liên kết kim loại không chỉ quyết định các tính chất vật lý và hóa học của kim loại mà còn ảnh hưởng sâu sắc đến sự phát triển của công nghệ và đời sống:
- Nền tảng của vật liệu kỹ thuật: Từ công trình xây dựng đồ sộ đến linh kiện điện tử phức tạp, tất cả đều dựa vào tính chất của liên kết kim loại.
- Ứng dụng đa dạng: Liên kết kim loại tạo ra những vật liệu có khả năng tái chế, góp phần xây dựng nền kinh tế tuần hoàn và bền vững.
- Thúc đẩy công nghệ mới: Các hợp kim và vật liệu mới dựa trên liên kết kim loại đang mở ra những hướng đi đầy hứa hẹn cho các ngành công nghiệp tương lai, ví dụ như vật liệu siêu dẫn, vật liệu nhẹ cho ngành hàng không, v.v.
6. So Sánh Liên Kết Kim Loại và Liên Kết Ion
Liên kết kim loại khác biệt hoàn toàn so với liên kết ion. Trong khi liên kết ion hình thành do sự trao đổi electron giữa kim loại và phi kim, tạo thành các ion trái dấu hút nhau, thì liên kết kim loại hình thành do sự chia sẻ electron giữa các nguyên tử kim loại trong một “biển electron” chung.
Liên kết ion tạo ra các hợp chất có tính chất giòn, dễ vỡ và thường là chất cách điện. Ngược lại, liên kết kim loại tạo ra các vật liệu dẻo, dễ uốn, có độ bền cao và khả năng dẫn điện, dẫn nhiệt tốt.
Tóm lại, liên kết kim loại là một yếu tố cốt lõi quyết định các tính chất vượt trội của kim loại. Hiểu rõ về liên kết kim loại giúp chúng ta khai thác và ứng dụng kim loại một cách hiệu quả hơn, góp phần vào sự phát triển của khoa học, công nghệ và kinh tế.