Kim loại sắt (Fe) là một nguyên tố quan trọng với nhiều ứng dụng trong đời sống và công nghiệp. Tuy nhiên, không phải dung dịch nào sắt cũng có thể phản ứng. Vậy, Kim Loại Fe Không Phản ứng Với những dung dịch nào và tại sao? Bài viết này sẽ cung cấp câu trả lời chi tiết, cùng với các kiến thức mở rộng và bài tập vận dụng để bạn đọc hiểu rõ hơn về tính chất hóa học của sắt.
Kim Loại Sắt Không Phản Ứng Với Dung Dịch Nào?
Câu hỏi thường gặp là: “Kim loại sắt không phản ứng được với dung dịch nào sau đây?”. Để trả lời, chúng ta cần xem xét tính chất hóa học của sắt và khả năng phản ứng của nó với các chất khác nhau.
Ví dụ, xét các lựa chọn sau:
A. ZnCl2.
B. FeCl3.
C. H2SO4 loãng, nguội.
D. AgNO3.
Đáp án đúng là A. ZnCl2.
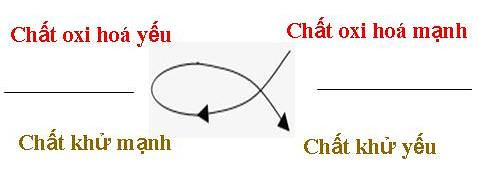 Quy tắc alpha áp dụng cho phản ứng của sắt với dung dịch muối
Quy tắc alpha áp dụng cho phản ứng của sắt với dung dịch muối
Theo quy tắc alpha, một kim loại chỉ phản ứng với dung dịch muối của kim loại yếu hơn nó trong dãy điện hóa. Sắt (Fe) đứng sau kẽm (Zn) trong dãy điện hóa, do đó, Fe không thể đẩy Zn ra khỏi dung dịch ZnCl2.
Giải Thích Chi Tiết
Để hiểu rõ hơn, chúng ta cần nắm vững các tính chất hóa học của sắt.
1. Tính Chất Hóa Học Của Sắt
Sắt là một kim loại có tính khử trung bình. Nó có thể tác dụng với nhiều chất khác nhau, bao gồm phi kim, axit và dung dịch muối.
1.1. Tác Dụng Với Phi Kim
Khi đun nóng, sắt tác dụng với hầu hết các phi kim:
-
Với oxi: 3Fe + 2O2 → Fe3O4 (Oxit sắt từ)
-
Với clo: 2Fe + 3Cl2 → 2FeCl3
1.2. Tác Dụng Với Axit
-
Với axit loãng (HCl, H2SO4 loãng): Sắt tác dụng tạo thành muối sắt (II) và giải phóng khí hidro.
- Fe + 2HCl → FeCl2 + H2↑
- Fe + H2SO4 → FeSO4 + H2↑
-
Với axit đặc, nguội (HNO3 đặc, nguội và H2SO4 đặc, nguội): Sắt không phản ứng do bị thụ động hóa. Lớp oxit trên bề mặt sắt ngăn cản phản ứng tiếp diễn.
-
Với axit đặc, nóng (HNO3 đặc, nóng và H2SO4 đặc, nóng): Sắt phản ứng tạo thành muối sắt (III), sản phẩm khử (NO2 hoặc SO2) và nước.
- Fe + 6HNO3 → Fe(NO3)3 + 3NO2 + 3H2O
- 2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
1.3. Tác Dụng Với Dung Dịch Muối
Sắt tác dụng với dung dịch muối của các kim loại kém hoạt động hơn nó trong dãy điện hóa.
- Ví dụ: Fe + CuSO4 → FeSO4 + Cu
Trường Hợp Đặc Biệt: Tính Thụ Động Hóa
Như đã đề cập, sắt không phản ứng với HNO3 đặc, nguội và H2SO4 đặc, nguội. Hiện tượng này được gọi là tính thụ động hóa. Nguyên nhân là do khi tiếp xúc với các axit này, trên bề mặt sắt hình thành một lớp oxit mỏng, bền, bảo vệ kim loại khỏi bị hòa tan.
Bài Tập Vận Dụng
Câu 1. Kim loại sắt không phản ứng được với dung dịch nào sau đây?
A. H2SO4 loãng
B. HNO3 loãng
C. HNO3 đặc nguội
D. H2SO4 đặc nóng
Đáp án: C. HNO3 đặc nguội
Câu 2. Sắt không phản ứng được với dung dịch nào sau đây?
A. Dung dịch chứa ion Ag+.
B. Dung dịch H2SO4 loãng.
C. Dung dịch HCl.
D. Dung dịch ZnSO4.
Đáp án: D. Dung dịch ZnSO4.
Câu 3. Cho một lá sắt vào dung dịch chứa đồng (II) sunfat. Hiện tượng quan sát được là:
A. Không có hiện tượng gì.
B. Lá sắt tan dần, dung dịch mất màu xanh.
C. Lá sắt tan dần, có khí thoát ra.
D. Lá sắt tan dần, có chất rắn màu đỏ bám vào lá sắt, dung dịch nhạt màu dần.
Đáp án: D. Lá sắt tan dần, có chất rắn màu đỏ bám vào lá sắt, dung dịch nhạt màu dần. (Fe + CuSO4 -> FeSO4 + Cu)
Kết Luận
Hiểu rõ các tính chất hóa học của sắt và quy tắc phản ứng giúp ta dễ dàng xác định kim loại Fe không phản ứng với dung dịch nào. Nắm vững kiến thức này không chỉ giúp bạn giải quyết các bài tập hóa học mà còn ứng dụng trong thực tế, đặc biệt trong các ngành công nghiệp liên quan đến kim loại và ăn mòn.