Kim loại Fe không phản ứng với dung dịch nào?
Câu hỏi “Kim Loại Fe Không Phản ứng Với Dung Dịch Nào Sau đây?” là một câu hỏi thường gặp trong chương trình hóa học phổ thông. Để trả lời câu hỏi này, chúng ta cần nắm vững tính chất hóa học của sắt (Fe) và các quy tắc phản ứng hóa học.
Thông thường, sắt có thể phản ứng với nhiều loại dung dịch axit, muối, và một số dung dịch oxi hóa mạnh. Tuy nhiên, có những trường hợp sắt không phản ứng, và việc xác định các trường hợp này rất quan trọng.
Giải thích chi tiết và đáp án
Xét ví dụ sau:
Câu hỏi: Kim loại Fe không phản ứng với dung dịch nào sau đây?
A. ZnCl2
B. FeCl3
C. H2SO4 loãng, nguội
D. AgNO3
Đáp án: A. ZnCl2
Giải thích:
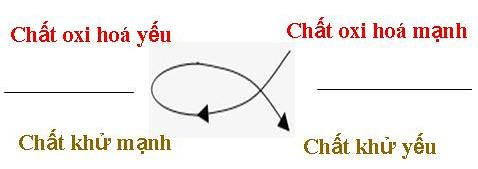 Quy tắc alpha cho phản ứng oxi hóa khử
Quy tắc alpha cho phản ứng oxi hóa khử
Theo quy tắc alpha trong hóa học, một kim loại chỉ có thể khử được ion kim loại đứng sau nó trong dãy điện hóa. Trong trường hợp này, Zn đứng trước Fe trong dãy điện hóa, do đó Fe không thể khử Zn2+ trong dung dịch ZnCl2. Hay nói cách khác, phản ứng không xảy ra.
Tính chất hóa học của Sắt (Fe)
Để hiểu rõ hơn về khả năng phản ứng của sắt, chúng ta cần xem xét các tính chất hóa học quan trọng của nó:
1. Tác dụng với phi kim
Sắt có thể phản ứng với nhiều phi kim, đặc biệt khi đun nóng.
-
Với Oxi:
3Fe + 2O2 → Fe3O4 (Oxit sắt từ)
-
Với Clo:
2Fe + 3Cl2 → 2FeCl3
Sản phẩm tạo thành phụ thuộc vào điều kiện phản ứng và lượng chất tham gia.
2. Tác dụng với Axit
-
Axit loãng (HCl, H2SO4 loãng):
Fe + 2HCl → FeCl2 + H2↑
Fe + H2SO4 → FeSO4 + H2↑
Trong các phản ứng này, sắt thể hiện hóa trị II.
-
Axit đặc, nóng (H2SO4 đặc, HNO3 đặc):
Fe + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
Fe + HNO3 đặc, nóng → Fe(NO3)3 + NO2 + H2O
Trong các phản ứng này, sắt thể hiện hóa trị III.
Lưu ý quan trọng: Sắt không phản ứng với HNO3 đặc nguội và H2SO4 đặc nguội do bị thụ động hóa.
3. Tác dụng với dung dịch muối
Sắt có thể phản ứng với dung dịch muối của các kim loại kém hoạt động hơn nó trong dãy điện hóa.
Fe + CuSO4 → FeSO4 + Cu
Các câu hỏi vận dụng
Câu 1: Kim loại sắt không phản ứng được với dung dịch nào sau đây?
A. H2SO4 loãng
B. HNO3 loãng
C. HNO3 đặc nguội
D. H2SO4 đặc nóng
Đáp án: C. HNO3 đặc nguội. Sắt bị thụ động hóa trong HNO3 đặc nguội.
Câu 2: Sắt tác dụng được với muối nào sau đây?
A. Zn(NO3)2
B. Mg(NO3)2
C. CuSO4
D. KCl
Đáp án: C. CuSO4. Vì Cu đứng sau Fe trong dãy điện hóa.
Phản ứng giữa đinh sắt và dung dịch CuSO4 tạo thành đồng (Cu) bám trên đinh sắt và dung dịch FeSO4.
Câu 3: Cho 11,2 gam bột sắt tác dụng với khí clo dư. Sau phản ứng thu được bao nhiêu gam muối sắt?
Giải:
2Fe + 3Cl2 → 2FeCl3
Số mol Fe = 11.2/56 = 0.2 mol
Số mol FeCl3 = Số mol Fe = 0.2 mol
Khối lượng FeCl3 = 0.2 * 162.5 = 32.5 gam
Kết luận
Việc nắm vững tính chất hóa học của sắt và các quy tắc phản ứng giúp chúng ta dễ dàng trả lời các câu hỏi liên quan đến khả năng phản ứng của sắt với các dung dịch khác nhau. Đặc biệt, cần lưu ý các trường hợp sắt không phản ứng do các yếu tố như thụ động hóa hoặc vị trí tương đối của các kim loại trong dãy điện hóa.
