Axit nitric (HNO3) là một hóa chất quan trọng được sử dụng rộng rãi trong nhiều ngành công nghiệp, từ sản xuất phân bón, thuốc nổ đến các hợp chất hữu cơ và vật liệu tẩy rửa. Vậy, quy trình điều Chế Hno3 Trong Công Nghiệp diễn ra như thế nào? Bài viết này sẽ cung cấp thông tin chi tiết về quy trình sản xuất, những lưu ý quan trọng khi sử dụng và địa chỉ mua HNO3 uy tín tại Việt Nam.
Các Phương Pháp Điều Chế Axit Nitric
1. Hình Thành HNO3 Trong Tự Nhiên
Axit nitric có thể hình thành tự nhiên trong các cơn mưa giông, khi có sự phóng điện từ sét. Tuy nhiên, lượng HNO3 tạo thành theo cách này là rất nhỏ và không đáng kể so với nhu cầu công nghiệp.
2. Điều Chế HNO3 Trong Phòng Thí Nghiệm
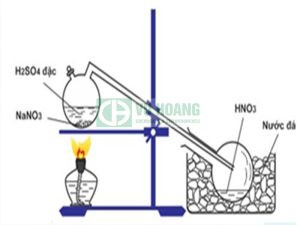
Trong phòng thí nghiệm, người ta có thể điều chế HNO3 bằng cách cho muối natri nitrat (NaNO3) tác dụng với axit sulfuric đặc (H2SO4) và chưng cất hỗn hợp. Phương trình phản ứng như sau:
H2SO4 (đặc) + NaNO3 (tinh thể) → HNO3 + NaHSO4
Một phương pháp khác là phân hủy nhiệt đồng (II) nitrat (Cu(NO3)2) để tạo ra khí nitơ dioxide (NO2) và oxy (O2). Sau đó, dẫn hỗn hợp khí này qua nước để thu được axit nitric.
2Cu(NO3)2 → 2CuO + 4NO2 + O2
4NO2 + O2 + 2H2O → 4HNO3
3. Điều Chế HNO3 Trong Công Nghiệp (Phương Pháp Ostwald)
Điều chế HNO3 trong công nghiệp chủ yếu dựa trên quy trình Ostwald, bao gồm các giai đoạn chính sau:
- Oxy hóa Amoniac: Amoniac (NH3) được oxy hóa bằng oxy (O2) trong không khí với xúc tác platin (Pt) ở nhiệt độ cao (850°C) để tạo thành nitơ monoxide (NO) và hơi nước.
4NH3 + 5O2 → 4NO + 6H2O (Pt, 850°C)
- Oxy hóa Nitơ Monoxide: Nitơ monoxide (NO) tiếp tục được oxy hóa bằng oxy (O2) để tạo thành nitơ dioxide (NO2).
2NO + O2 → 2NO2
- Hấp thụ Nitơ Dioxide: Nitơ dioxide (NO2) được hấp thụ trong nước để tạo thành axit nitric (HNO3).
4NO2 + O2 + 2H2O → 4HNO3
Dung dịch axit nitric thu được thường có nồng độ khoảng 52% đến 68%. Để đạt được nồng độ cao hơn, có thể thực hiện quá trình chưng cất với axit sulfuric (H2SO4) để loại bỏ nước.
Lưu Ý Khi Sử Dụng Axit Nitric
- Axit nitric là một chất oxy hóa mạnh, có thể gây cháy nổ khi tiếp xúc với các chất hữu cơ, kim loại, hoặc cyanit.
- Axit nitric đậm đặc gây bỏng da nghiêm trọng do phản ứng với protein. Khi tiếp xúc với da, nó sẽ làm da chuyển sang màu vàng.
- Khi pha loãng axit nitric, luôn đổ từ từ axit vào nước, không đổ nước vào axit để tránh gây bắn và nổ.
Lưu Trữ Axit Nitric An Toàn
- Lưu trữ axit nitric trong khu vực khô ráo, thoáng mát, tránh xa các chất dễ cháy, chất hữu cơ, kim loại và nguồn nhiệt.
- Sử dụng thùng chứa bằng nhựa hoặc vật liệu chống ăn mòn khác.
- Đảm bảo khu vực lưu trữ có nền chống axit.
- Các thùng chứa phải được đậy kín để tránh rò rỉ và tiếp xúc với không khí.
Địa Chỉ Mua Axit Nitric (HNO3) Uy Tín
Nếu bạn đang tìm kiếm nguồn cung cấp axit nitric (HNO3) chất lượng và uy tín, hãy liên hệ với Công ty TNHH Công nghệ Hóa chất và Môi trường Vũ Hoàng. Chúng tôi là nhà cung cấp hàng đầu các loại hóa chất công nghiệp, hóa chất tinh khiết, đảm bảo chất lượng sản phẩm và dịch vụ tốt nhất.
Thông tin liên hệ:
- Hotline: 0945609898 (Mr Huy)
- Điện thoại: 024 3382 9999 – 0857829999
- Website: https://vuhoangco.com.vn
- Email: [email protected]
- Địa chỉ: Lô H1-2, KCN Đại Đồng- Hoàn Sơn, Xã Tri Phương, Huyện Tiên Du, Bắc Ninh
- Văn phòng đại diện: Tầng 7, Tòa nhà Cotana Lô CC5A Bán đảo Linh Đàm, phường Hoàng Liệt, quận Hoàng Mai, Hà Nội