Axetilen (C2H2), hay còn gọi là ethyne theo danh pháp IUPAC, là một hydrocacbon không no thuộc dãy đồng đẳng ankin, có vai trò quan trọng trong nhiều lĩnh vực công nghiệp và đời sống. Bài viết này sẽ cung cấp thông tin chi tiết và toàn diện về Ctpt Axetilen, bao gồm tính chất, phương pháp điều chế, ứng dụng và các lưu ý quan trọng khi sử dụng.
1. Axetilen (C2H2) là gì?
Axetilen là một hợp chất hữu cơ với công thức phân tử C2H2. Nó là ankin đơn giản nhất, với một liên kết ba giữa hai nguyên tử cacbon.
Công thức cấu tạo của axetilen: H-C≡C-H
Một số tên gọi khác: Ethyne
2. Lịch sử phát hiện Axetilen
- 1836: Edmund Davy phát hiện ra axetilen khi thử nghiệm với cacbua kali.
- 1859: Marcel Morren tạo ra axetilen bằng cách sử dụng điện cực cacbon trong môi trường hydro.
- 1860: Marcellin Berthelot tái xuất hiện và đặt tên cho axetilen là “acétylène”.
3. Tính chất đặc trưng của CTPT Axetilen (C2H2)
3.1. Tính chất vật lý
- Axetilen là chất khí không màu, không mùi (khi tinh khiết). Axetilen thương mại thường có mùi khó chịu do lẫn tạp chất.
- Ít tan trong nước.
- Nhẹ hơn không khí (tỉ trọng so với không khí là 26/29).
- Dễ cháy và tạo thành hỗn hợp nổ với không khí.
3.2. Tính chất hóa học
-
Phản ứng cháy:
2 C2H2 + 5 O2 → 4 CO2 + 2 H2O (phản ứng tỏa nhiệt mạnh)
-
Phản ứng cộng:
-
Cộng halogen:
HC≡CH + Br2 → BrCH=CHBr (đibromoetilen)
BrCH=CHBr + Br2 → Br2CH-CHBr2 (tetrabromoetan)
-
Cộng hidro halogenua:
HC≡CH + HCl → CH2=CHCl (vinyl clorua)
-
Cộng nước (hidrat hóa): Xúc tác HgSO4, tạo thành axetaldehyt.
HC≡CH + H2O → CH3CHO
-
Phản ứng với dung dịch AgNO3/NH3: Tạo kết tủa vàng.
HC≡CH + 2AgNO3 + 2NH3 → AgC≡CAg ↓ + 2NH4NO3
-
-
Phản ứng dime hóa và trime hóa:
- Dime hóa: 2HC≡CH → CH≡C-CH=CH2 (vinyl axetilen)
- Trime hóa: 3HC≡CH → C6H6 (benzen)
-
Phản ứng trùng hợp:
nHC≡CH → (-CH=CH-)n (poliaxetilen)
4. Điều chế Axetilen
4.1. Trong phòng thí nghiệm
Cho canxi cacbua (CaC2) tác dụng với nước:
CaC2 + 2H2O → C2H2 + Ca(OH)2
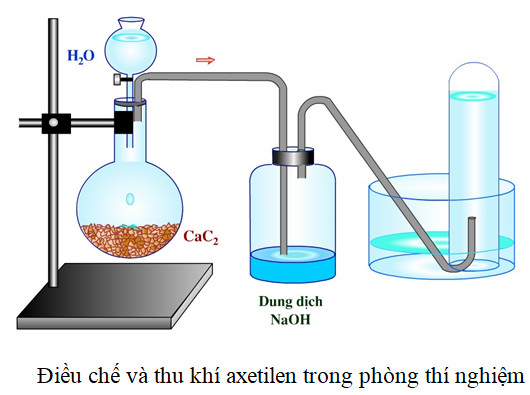 Điều chế axetilen từ canxi cacbua và nước trong phòng thí nghiệm.
Điều chế axetilen từ canxi cacbua và nước trong phòng thí nghiệm.
Sơ đồ thí nghiệm điều chế axetilen trong phòng thí nghiệm, sử dụng phản ứng giữa canxi cacbua và nước.
4.2. Trong công nghiệp
-
Nhiệt phân metan ở nhiệt độ cao (1500°C):
2 CH4 → C2H2 + 3 H2
-
Oxi hóa không hoàn toàn metan:
2CH4 + O2 → 2CO + 4H2
-
Điện phân dung dịch muối:
2C + H2 (hồ quang điện) → C2H2
5. Ứng dụng của Axetilen
-
Sản xuất hóa chất: Axetilen là nguyên liệu quan trọng để sản xuất nhiều hợp chất hữu cơ khác như vinyl clorua (sản xuất PVC), vinyl axetat, acrylonitrile (sản xuất sợi tổng hợp), axetaldehyt, axit axetic,…
-
Nhiên liệu: Axetilen được sử dụng trong đèn hàn cắt kim loại (đèn xì axetilen) khi đốt với oxy, tạo ra ngọn lửa có nhiệt độ cao.
Công nhân sử dụng đèn xì oxi-axetilen để hàn kim loại, thể hiện ứng dụng quan trọng của axetilen trong công nghiệp.
-
Sản xuất polymer: Trùng hợp axetilen tạo thành poliaxetilen, một loại polymer dẫn điện.
-
Trong nông nghiệp: Axetilen được sử dụng để thúc đẩy quá trình chín của trái cây.
6. Axetilen có độc không? Lưu ý khi sử dụng
- Axetilen không quá độc, nhưng ở nồng độ cao có thể gây ngạt thở do thiếu oxy.
- Axetilen là chất dễ cháy nổ, đặc biệt khi trộn lẫn với không khí hoặc oxy.
- Lưu ý khi sử dụng:
- Làm việc trong môi trường thông thoáng.
- Tránh xa nguồn nhiệt và lửa.
- Bảo quản axetilen trong bình chứa chuyên dụng, tránh va đập mạnh.
- Không sử dụng bình axetilen đã quá hạn.
7. Bài tập vận dụng về Axetilen
Bài 1: Đốt cháy hoàn toàn 2.24 lít khí axetilen (đktc). Tính thể tích khí CO2 thu được.
Giải:
nC2H2 = 2.24/22.4 = 0.1 mol
2 C2H2 + 5 O2 → 4 CO2 + 2 H2O
Theo phương trình, nCO2 = 2 * nC2H2 = 0.2 mol
VCO2 = 0.2 * 22.4 = 4.48 lít
Bài 2: Dẫn 0.2 mol khí axetilen qua dung dịch AgNO3/NH3 dư. Tính khối lượng kết tủa thu được.
Giải:
HC≡CH + 2AgNO3 + 2NH3 → AgC≡CAg ↓ + 2NH4NO3
Theo phương trình, nAgC≡CAg = nC2H2 = 0.2 mol
M(AgC≡CAg) = 240 g/mol
m(AgC≡CAg) = 0.2 * 240 = 48 gam
8. Mua Axetilen ở đâu uy tín, chất lượng?
Việc lựa chọn nhà cung cấp uy tín là yếu tố then chốt để đảm bảo chất lượng và an toàn khi sử dụng axetilen. Các bạn có thể tìm đến các công ty chuyên cung cấp hóa chất công nghiệp có uy tín trên thị trường.
Hy vọng bài viết này đã cung cấp cho bạn những thông tin đầy đủ và chi tiết về ctpt axetilen. Nắm vững kiến thức về axetilen sẽ giúp bạn ứng dụng hiệu quả và an toàn hợp chất này trong công việc và cuộc sống.