Este là một hợp chất hữu cơ quan trọng, có nhiều ứng dụng trong đời sống và công nghiệp. Bài viết này sẽ cung cấp một cái nhìn toàn diện về Công Thức Este, cách phân loại, điều chế và những ứng dụng quan trọng của chúng.
1. Định Nghĩa Este và Công Thức Tổng Quát
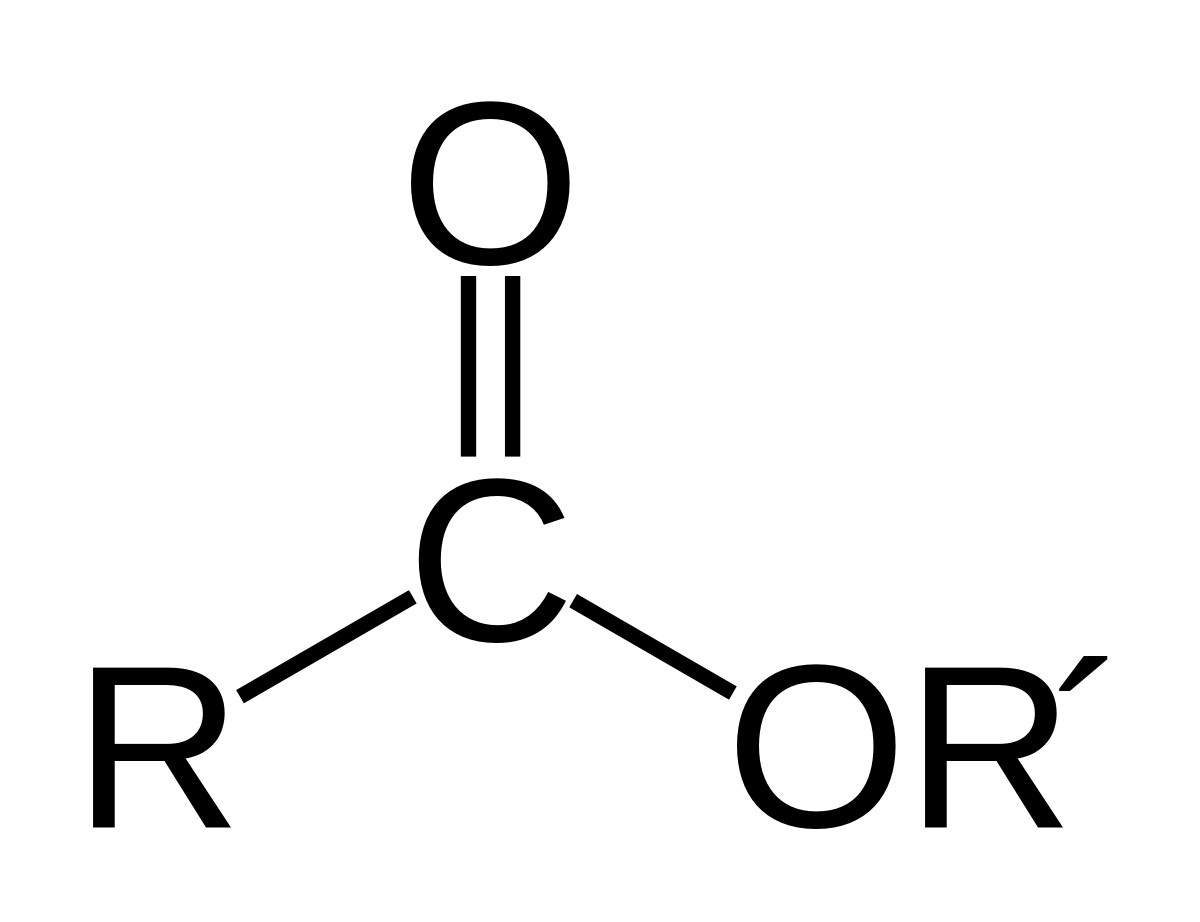
Este là sản phẩm thu được khi thay thế nhóm -OH trong nhóm carboxyl (-COOH) của axit cacboxylic bằng nhóm -OR’ (với R’ là gốc hiđrocacbon).
Công thức tổng quát của este đơn chức là: RCOOR’, trong đó:
- R là gốc hiđrocacbon của axit (hoặc H đối với axit fomic).
- R’ là gốc hiđrocacbon của ancol (R’ ≠ H).
Công thức tổng quát của este no, đơn chức, mạch hở:
- CnH2nO2 (n ≥ 2)
- CnH2n+1COOCmH2m+1 (n ≥ 0, m ≥ 1)
2. Danh Pháp (Cách Gọi Tên) Este
Tên của este được hình thành theo cấu trúc sau: Tên gốc hiđrocacbon R’ (từ ancol) + Tên gốc axit (đuôi “at”).
Ví dụ:
- HCOOCH3: Metyl fomat (axit fomic tạo gốc fomat, ancol metylic tạo gốc metyl)
- CH3COOC2H5: Etyl axetat (axit axetic tạo gốc axetat, ancol etylic tạo gốc etyl)
- CH2=CHCOOCH3: Metyl acrylat (axit acrylic tạo gốc acrylat, ancol metylic tạo gốc metyl)
Lưu ý: Với ancol đa chức, tên este được gọi là: Tên ancol + Tên gốc axit. Ví dụ: (CH3COO)2C2H4 là etylen glycol điaxetat.
3. Phân Loại Este
Este được phân loại dựa trên cấu trúc của gốc hiđrocacbon và số lượng nhóm chức:
- Este no, đơn chức: CnH2nO2 (n ≥ 2). Ví dụ: CH3COOC2H5 (etyl axetat).
- Este không no, đơn chức: CmH2m+2-2kO2 (k ≥ 2, k là số liên kết pi). Ví dụ: CH2=CH-COOCH3 (metyl acrylat).
- Este đa chức:
- Este tạo bởi axit đơn chức và ancol đa chức: (RCOO)mR’.
- Este tạo bởi axit đa chức và ancol đơn chức: R(COOR’)m.
- Este tạo bởi axit đa chức và ancol đa chức: Rm(COO)nmR’n.
4. Tính Chất Vật Lý của Este
- Trạng thái: Thường là chất lỏng ở điều kiện thường. Este có khối lượng phân tử lớn có thể tồn tại ở trạng thái rắn (như sáp ong, mỡ động vật).
- Nhiệt độ sôi: Thấp hơn so với ancol và axit cacboxylic có cùng khối lượng phân tử do không tạo được liên kết hiđro giữa các phân tử.
- Độ tan: Ít tan hoặc không tan trong nước do không tạo được liên kết hiđro với nước.
- Mùi: Nhiều este có mùi thơm đặc trưng của hoa quả. Ví dụ:
- Isoamyl axetat (CH3COOCH2CH2(CH3)2): mùi chuối.
- Etyl butirat (CH3CH2CH2COOC2H5): mùi dứa.
- Geranyl axetat (CH3COOC10H17): mùi hoa hồng.
5. Tính Chất Hóa Học của Este
- Phản ứng thủy phân:
- Trong môi trường axit (xúc tác H+, t°): RCOOR’ + H2O ⇌ RCOOH + R’OH (phản ứng thuận nghịch)
- Trong môi trường kiềm (phản ứng xà phòng hóa): RCOOR’ + NaOH → RCOONa + R’OH (phản ứng một chiều)
- Phản ứng khử: Este bị khử bởi LiAlH4 tạo thành ancol bậc nhất.
- Phản ứng cộng và trùng hợp (ở gốc hiđrocacbon không no): Tương tự như anken, este có gốc không no có thể tham gia phản ứng cộng H2, Br2, trùng hợp,…
Hình ảnh này minh họa phản ứng khử este, một phản ứng quan trọng trong hóa học hữu cơ, giúp người học hiểu rõ hơn về sự biến đổi của este dưới tác dụng của chất khử.
Lưu ý:
- Este của phenol khi thủy phân trong môi trường kiềm tạo ra 2 muối và nước: RCOOC6H5 + 2NaOH → RCOONa + C6H5ONa + H2O
- Este của axit fomic (HCOO-) có khả năng tham gia phản ứng tráng gương.
6. Điều Chế Este
-
Phản ứng este hóa (điều chế este của ancol): Đun hồi lưu axit cacboxylic với ancol, xúc tác H2SO4 đặc.
RCOOH + R’OH ⇌ RCOOR’ + H2O
Để tăng hiệu suất phản ứng, có thể tăng nồng độ chất tham gia hoặc giảm nồng độ sản phẩm (chưng cất este hoặc dùng H2SO4 đặc để hút nước).
-
Điều chế este của phenol: Cho anhidrit axit hoặc clorua axit tác dụng với phenol.
(CH3CO)2O + C6H5OH → CH3COOC6H5 + CH3COOH
7. Ứng Dụng của Este
- Dung môi: Nhiều este được sử dụng làm dung môi trong công nghiệp sơn, mực in,…
- Sản xuất polyme: Sản xuất các polyme quan trọng như poli(metyl acrylat), poli(metyl metacrylat) (thủy tinh hữu cơ), poli(vinyl axetat) (chất dẻo, keo dán).
- Chất hóa dẻo: Một số este của axit phtalic được dùng làm chất hóa dẻo.
- Hương liệu, thực phẩm, mỹ phẩm: Nhiều este có mùi thơm đặc trưng được sử dụng trong công nghiệp thực phẩm và mỹ phẩm.
8. Nhận Biết Este
- Este của axit fomic: Tham gia phản ứng tráng gương.
- Este không no: Làm mất màu dung dịch brom.
- Thủy phân este của glixerol (chất béo): Sản phẩm hòa tan Cu(OH)2 tạo dung dịch xanh lam.
- Thủy phân este tạo anđehit: Tham gia phản ứng tráng gương.
Hy vọng bài viết này đã cung cấp cho bạn một cái nhìn tổng quan và chi tiết về công thức este, từ định nghĩa, phân loại, tính chất đến điều chế và ứng dụng. Nắm vững kiến thức về este sẽ giúp bạn học tốt môn Hóa học và hiểu rõ hơn về các ứng dụng của chúng trong đời sống.