Este là một hợp chất hữu cơ quan trọng, có mặt trong nhiều lĩnh vực của đời sống và hóa học. Để hiểu rõ về este, đặc biệt là este no đơn chức mạch hở, chúng ta cần nắm vững công thức chung, cách gọi tên và các tính chất đặc trưng. Bài viết này sẽ cung cấp một cái nhìn toàn diện về chủ đề này, giúp bạn nắm bắt kiến thức một cách hệ thống và hiệu quả.
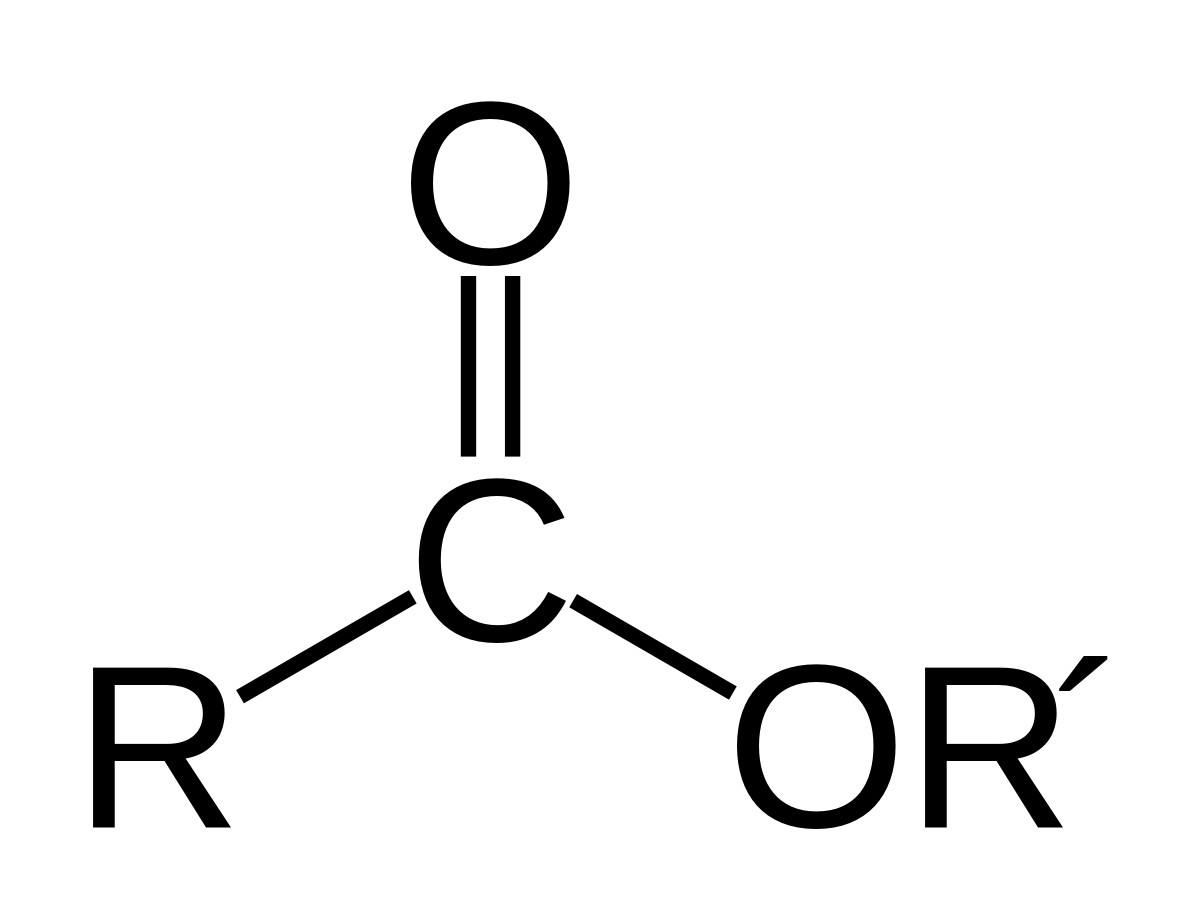
Khi thay nhóm OH trong nhóm cacboxyl của axit cacboxylic bằng nhóm OR thì thu được một este. Công thức chung của este đơn chức là R-COO-R’.
Trong đó R là gốc hidrocacbon của axit (hoặc là H với axit fomic), còn R’ là gốc hiđrocacbon của ancol (với R không phải H).
Công Thức Chung Của Este No Đơn Chức Mạch Hở
Este no, đơn chức, mạch hở là loại este phổ biến nhất. Chúng được tạo thành từ axit cacboxylic no, đơn chức và ancol no, đơn chức.
Công thức chung của este no, đơn chức, mạch hở là:
- CₙH₂ₙO₂ (với n ≥ 2)
Ngoài ra, công thức cấu tạo tổng quát có thể được biểu diễn như sau:
- R-COO-R’
Trong đó:
- R là gốc alkyl no, đơn chức (CₙH₂ₙ₊₁) hoặc H (trong trường hợp este của axit fomic).
- R’ là gốc alkyl no, đơn chức (CₘH₂ₘ₊₁).
Ví dụ: CH₃COOCH₃ (metyl axetat), C₂H₅COOC₂H₅ (etyl propionat)…
Cách Gọi Tên Este (Danh Pháp)
Tên este được hình thành bằng cách ghép tên gốc alkyl của ancol (R’) với tên gốc acyl của axit cacboxylic (RCOO), thêm đuôi “-at”.
Tên este = Tên gốc alkyl (R’) + Tên gốc axit (RCOO) + “at”
Ví dụ:
- HCOOCH₃: Metyl fomat (gốc CH₃ là metyl, gốc HCOO là fomat)
- CH₃COOC₂H₅: Etyl axetat (gốc C₂H₅ là etyl, gốc CH₃COO là axetat)
Tính Chất Vật Lý Của Este
- Trạng thái: Ở điều kiện thường, este thường ở trạng thái lỏng. Các este có khối lượng phân tử lớn có thể ở trạng thái rắn (ví dụ: sáp ong).
- Mùi: Nhiều este có mùi thơm dễ chịu, ví dụ như mùi trái cây.
- Độ tan: Este ít tan trong nước do không tạo được liên kết hydro với nước. Chúng tan tốt trong các dung môi hữu cơ.
- Nhiệt độ sôi: Este có nhiệt độ sôi thấp hơn so với axit cacboxylic và ancol có cùng khối lượng phân tử, do không có liên kết hydro giữa các phân tử este.
Tính Chất Hóa Học Của Este No Đơn Chức Mạch Hở
Este tham gia vào một số phản ứng hóa học quan trọng:
- Phản ứng thủy phân:
- Trong môi trường axit (H⁺, t°):
RCOOR’ + H₂O ⇌ RCOOH + R’OH (phản ứng thuận nghịch) - Trong môi trường kiềm (NaOH, t°): (phản ứng xà phòng hóa)
RCOOR’ + NaOH → RCOONa + R’OH (phản ứng một chiều)
- Trong môi trường axit (H⁺, t°):
- Phản ứng đốt cháy:
CₙH₂ₙO₂ + (3n-2)/2 O₂ → nCO₂ + nH₂O - Phản ứng khử: Este có thể bị khử bởi các chất khử mạnh như LiAlH₄ tạo thành ancol bậc nhất.
Điều Chế Este No Đơn Chức Mạch Hở
Phương pháp điều chế este phổ biến nhất là phản ứng este hóa giữa axit cacboxylic và ancol, có xúc tác là axit sulfuric đặc (H₂SO₄ đặc).
RCOOH + R’OH ⇌ RCOOR’ + H₂O
Để tăng hiệu suất phản ứng, người ta thường sử dụng dư một trong hai chất phản ứng (axit hoặc ancol) hoặc loại bỏ sản phẩm (este hoặc nước) khỏi hỗn hợp phản ứng.
Ứng Dụng Của Este
Este có nhiều ứng dụng quan trọng trong đời sống và công nghiệp:
- Dung môi: Este được sử dụng làm dung môi trong nhiều quá trình công nghiệp, ví dụ như trong sản xuất sơn, mực in, keo dán…
- Hương liệu: Nhiều este có mùi thơm dễ chịu, được sử dụng trong công nghiệp thực phẩm, mỹ phẩm và sản xuất nước hoa.
- Sản xuất polymer: Một số este là monomer để sản xuất các polymer quan trọng như poly(vinyl axetat) (PVA) và poly(metyl metacrylat) (PMMA).
- Chất hóa dẻo: Một số este được sử dụng làm chất hóa dẻo trong sản xuất nhựa.
Nắm vững công thức chung, cách gọi tên, tính chất và ứng dụng của este no đơn chức mạch hở là nền tảng quan trọng để học tốt hóa học hữu cơ. Hy vọng bài viết này đã cung cấp cho bạn những kiến thức hữu ích và cần thiết.