Cấu hình electron nguyên tử là một khái niệm quan trọng trong hóa học, giúp chúng ta hiểu rõ sự phân bố electron trong nguyên tử. Từ cấu hình electron, chúng ta có thể dễ dàng xác định được số lớp electron của một nguyên tố. Bài viết này sẽ tập trung vào Cách Xác định Số Lớp Electron một cách chi tiết và dễ hiểu nhất.
Cấu hình electron nguyên tử biểu diễn sự phân bố các electron trong lớp vỏ nguyên tử ở các trạng thái năng lượng khác nhau, hay ở các vùng không gian mà electron có khả năng tồn tại cao nhất. Nói một cách đơn giản, nó cho biết các electron được sắp xếp như thế nào trong các lớp và phân lớp quanh hạt nhân.
Ví dụ về cấu hình electron của một vài nguyên tố thường gặp:
| Nguyên tố | Z | Cấu hình e | Số lớp electron |
|---|---|---|---|
| K (Kali) | 19 | 1s22s22p63s23p64s1 | 4 |
| Ca (Canxi) | 20 | 1s22s22p63s23p64s2 | 4 |
| Al (Nhôm) | 13 | 1s22s22p63s23p1 | 3 |
| Fe (Sắt) | 26 | 1s22s22p63s23p63d64s2 | 4 |
| Cu (Đồng) | 29 | 1s22s22p63s23p63d104s1 | 4 |
| Cr (Crom) | 24 | 1s22s22p63s23p63d54s1 | 4 |

Để xác định số lớp electron, chúng ta cần hiểu rõ về cấu trúc lớp vỏ electron.
Cấu Trúc Lớp Vỏ Electron
Trong nguyên tử, các electron được sắp xếp thành các lớp (hay còn gọi là mức năng lượng chính) xung quanh hạt nhân. Các lớp này được đánh số từ 1 đến 7, tương ứng với các chữ cái K, L, M, N, O, P, Q.
- Lớp 1 (K): Gần hạt nhân nhất, có mức năng lượng thấp nhất và chứa tối đa 2 electron.
- Lớp 2 (L): Chứa tối đa 8 electron.
- Lớp 3 (M): Chứa tối đa 18 electron.
- Lớp 4 (N): Chứa tối đa 32 electron.
- Lớp 5 (O), 6 (P), 7 (Q): Cũng có thể chứa tối đa 32 electron, nhưng trong thực tế, các nguyên tố có số electron lớn thường không đạt đến con số này.
Mỗi lớp electron lại bao gồm các phân lớp (hay còn gọi là mức năng lượng phụ), ký hiệu là s, p, d, và f.
- Phân lớp s: Chứa tối đa 2 electron.
- Phân lớp p: Chứa tối đa 6 electron.
- Phân lớp d: Chứa tối đa 10 electron.
- Phân lớp f: Chứa tối đa 14 electron.
Cấu trúc lớp vỏ electron với các lớp (K, L, M,…) và phân lớp (s, p, d,…) được mô tả trực quan, giúp người đọc dễ dàng hình dung cách electron phân bố trong nguyên tử.
Cách Xác Định Số Lớp Electron
Cách xác định số lớp electron rất đơn giản:
-
Viết cấu hình electron: Xác định số electron của nguyên tử (bằng số proton, Z). Sau đó, viết cấu hình electron đầy đủ của nguyên tử đó.
-
Đếm số lớp electron: Số lớp electron của một nguyên tử bằng số lớn nhất đứng trước ký hiệu của phân lớp trong cấu hình electron.
Ví dụ:
- Nguyên tử Natri (Na) có Z = 11. Cấu hình electron là 1s22s22p63s1. Số lớn nhất đứng trước ký hiệu phân lớp là 3. Vậy, Natri có 3 lớp electron.
- Nguyên tử Sắt (Fe) có Z = 26. Cấu hình electron là 1s22s22p63s23p63d64s2. Số lớn nhất đứng trước ký hiệu phân lớp là 4. Vậy, Sắt có 4 lớp electron.
Ví Dụ Minh Họa
Để hiểu rõ hơn về cách xác định số lớp electron, hãy xem xét thêm một vài ví dụ:
- Oxy (O, Z = 8): Cấu hình electron là 1s22s22p4. Số lớp electron là 2.
- Clo (Cl, Z = 17): Cấu hình electron là 1s22s22p63s23p5. Số lớp electron là 3.
- Canxi (Ca, Z = 20): Cấu hình electron là 1s22s22p63s23p64s2. Số lớp electron là 4.
Bảng Cấu Hình Electron và Số Lớp Electron của 20 Nguyên Tố Đầu Tiên
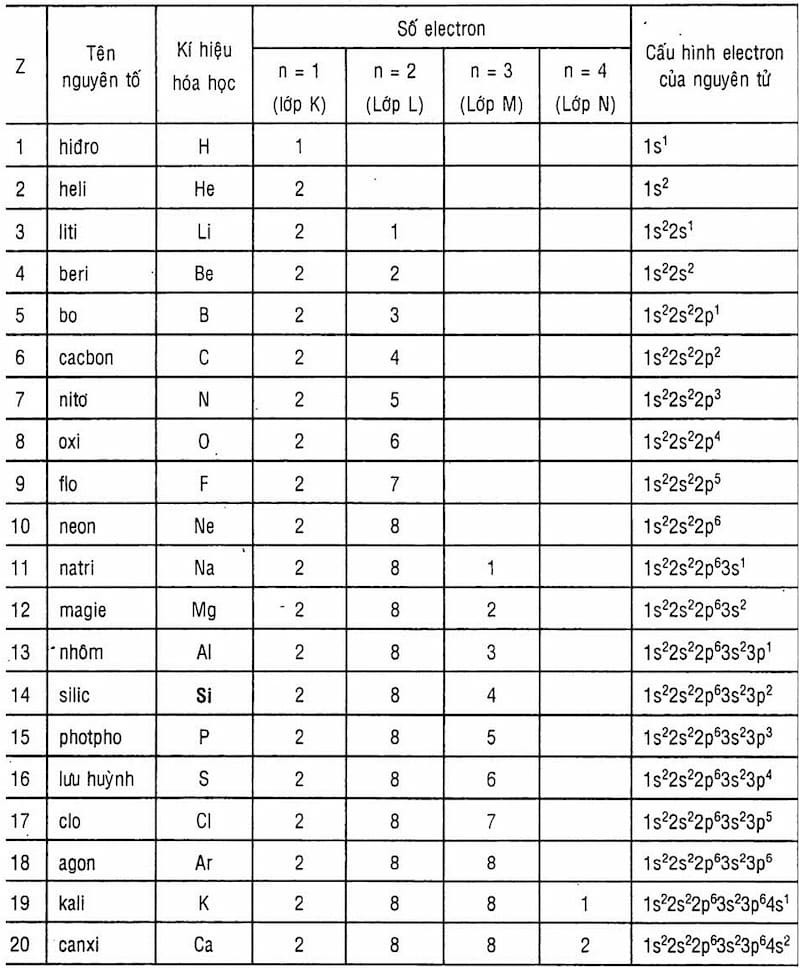
Để tham khảo nhanh, dưới đây là bảng cấu hình electron và số lớp electron của 20 nguyên tố đầu tiên trong bảng tuần hoàn:
| Z | Nguyên tố | Cấu hình electron | Số lớp electron |
|---|---|---|---|
| 1 | Hiđro (H) | 1s1 | 1 |
| 2 | Heli (He) | 1s2 | 1 |
| 3 | Liti (Li) | 1s22s1 | 2 |
| 4 | Beri (Be) | 1s22s2 | 2 |
| 5 | Bo (B) | 1s22s22p1 | 2 |
| 6 | Cacbon (C) | 1s22s22p2 | 2 |
| 7 | Nitơ (N) | 1s22s22p3 | 2 |
| 8 | Oxy (O) | 1s22s22p4 | 2 |
| 9 | Flo (F) | 1s22s22p5 | 2 |
| 10 | Neon (Ne) | 1s22s22p6 | 2 |
| 11 | Natri (Na) | 1s22s22p63s1 | 3 |
| 12 | Magie (Mg) | 1s22s22p63s2 | 3 |
| 13 | Nhôm (Al) | 1s22s22p63s23p1 | 3 |
| 14 | Silic (Si) | 1s22s22p63s23p2 | 3 |
| 15 | Photpho (P) | 1s22s22p63s23p3 | 3 |
| 16 | Lưu huỳnh (S) | 1s22s22p63s23p4 | 3 |
| 17 | Clo (Cl) | 1s22s22p63s23p5 | 3 |
| 18 | Argon (Ar) | 1s22s22p63s23p6 | 3 |
| 19 | Kali (K) | 1s22s22p63s23p64s1 | 4 |
| 20 | Canxi (Ca) | 1s22s22p63s23p64s2 | 4 |
Bảng thống kê cấu hình electron và số lớp electron của 20 nguyên tố đầu tiên, giúp học sinh dễ dàng tra cứu và học thuộc.
Ý Nghĩa của Số Lớp Electron
Số lớp electron có vai trò quan trọng trong việc xác định tính chất hóa học của một nguyên tố. Các electron ở lớp ngoài cùng (lớp hóa trị) quyết định khả năng tham gia liên kết hóa học của nguyên tố đó.
- Nguyên tố có số lớp electron ít thường có xu hướng dễ dàng nhường hoặc nhận electron để đạt cấu hình bền vững.
- Các nguyên tố cùng nhóm trong bảng tuần hoàn có số electron lớp ngoài cùng giống nhau, do đó có tính chất hóa học tương tự.
Bài Tập Vận Dụng
Để củng cố kiến thức về cách xác định số lớp electron, hãy thử giải các bài tập sau:
- Viết cấu hình electron của nguyên tử Đồng (Cu, Z = 29) và xác định số lớp electron.
- Nguyên tố X có cấu hình electron là 1s22s22p63s23p64s1. Xác định số lớp electron của nguyên tố X.
- Nguyên tố Y có 3 lớp electron và 5 electron ở lớp ngoài cùng. Xác định cấu hình electron của nguyên tố Y.
Kết Luận
Hiểu rõ về cấu hình electron và cách xác định số lớp electron là nền tảng quan trọng để nắm vững kiến thức hóa học. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích và dễ hiểu nhất về chủ đề này. Chúc bạn học tốt!

