1. Axit: Khái Niệm, Phân Loại và Cách Gọi Tên
Axit là hợp chất hóa học quan trọng, đóng vai trò then chốt trong nhiều phản ứng và ứng dụng khác nhau. Để hiểu rõ về axit, chúng ta cần nắm vững các khái niệm cơ bản, cách phân loại và quy tắc gọi tên.
a. Khái niệm:
Axit là phân tử chứa một hoặc nhiều nguyên tử hydro (H) liên kết với gốc axit. Các nguyên tử hydro này có khả năng thay thế bằng các nguyên tử kim loại. Tính chất này quyết định khả năng tác dụng của axit với nhiều chất khác nhau.
b. Công thức hóa học (CTHH):
Công thức chung của axit bao gồm một hay nhiều nguyên tử H và gốc axit. Ví dụ: HCl, H2SO4, HNO3.
c. Phân loại:
Có hai loại axit chính dựa trên thành phần nguyên tố:
- Axit không có oxi: Là axit mà phân tử không chứa nguyên tử oxi (O). Ví dụ: HCl (axit clohidric), H2S (axit sunfuhidric).
- Axit có oxi: Là axit mà phân tử có chứa nguyên tử oxi (O). Ví dụ: H2SO4 (axit sunfuric), HNO3 (axit nitric), H2CO3 (axit cacbonic).
d. Tên gọi:
Việc gọi tên axit phụ thuộc vào loại axit (có oxi hay không có oxi) và số lượng oxi trong gốc axit.
-
Axit không có oxi:
Tên axit = axit + tên phi kim + hidric
Ví dụ:
- HCl: axit clohidric (gốc axit tương ứng là clorua)
- H2S: axit sunfuhidric (gốc axit tương ứng là sunfua)
-
Axit có oxi:
-
Axit có nhiều oxi:
Tên axit = axit + tên phi kim + ic
Ví dụ:
- H2SO4: axit sunfuric (gốc axit: sunfat)
- HNO3: axit nitric (gốc axit: nitrat)
-
Axit có ít oxi:
Tên axit = axit + tên phi kim + ơ
Ví dụ:
- H2SO3: axit sunfuro (gốc axit: sunfit)
-
2. Bazơ: Khái Niệm, Phân Loại và Cách Gọi Tên
Bazơ, hay còn gọi là kiềm, là một loại hợp chất hóa học có khả năng nhận proton (H+). Chúng có những tính chất đặc trưng và ứng dụng rộng rãi trong đời sống và công nghiệp.
a. Khái niệm:
Bazơ là phân tử gồm một nguyên tử kim loại liên kết với một hoặc nhiều nhóm hidroxit (-OH). Nhóm hidroxit là yếu tố quyết định tính bazơ của hợp chất.
b. Công thức hóa học (CTHH):
Công thức chung của bazơ là M(OH)n, trong đó M là kim loại và n là hóa trị của kim loại.
c. Tên gọi:
Tên bazơ = tên kim loại (kèm hóa trị nếu có nhiều hóa trị) + hidroxit
Ví dụ:
- Fe(OH)2: sắt (II) hidroxit
- KOH: kali hidroxit
- NaOH: natri hidroxit
d. Phân loại:
Bazơ được phân loại dựa trên khả năng tan trong nước:
- Bazơ tan (kiềm): Các bazơ này tan tốt trong nước, tạo thành dung dịch có tính kiềm mạnh. Ví dụ: NaOH, KOH, Ca(OH)2, Ba(OH)2.
- Bazơ không tan: Các bazơ này ít hoặc không tan trong nước. Ví dụ: Cu(OH)2, Fe(OH)2, Fe(OH)3.
3. Muối: Khái Niệm, Phân Loại và Cách Gọi Tên
Muối là hợp chất hóa học được tạo thành khi các ion kim loại liên kết với các gốc axit. Chúng là thành phần quan trọng trong nhiều quá trình hóa học và sinh học.
a. Khái niệm:
Muối là phân tử có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit.
b. Công thức hóa học (CTHH):
Công thức hóa học của muối gồm hai phần: kim loại và gốc axit.
Ví dụ: Na2SO4, CaCO3, NaCl
c. Tên gọi:
Tên muối = tên kim loại (kèm hóa trị nếu có nhiều hóa trị) + tên gốc axit
Ví dụ:
- Na2SO4: natri sunfat
- CaCO3: canxi cacbonat
- FeSO4: sắt (II) sunfat
d. Phân loại:
Muối được phân loại dựa trên khả năng thay thế nguyên tử hydro trong gốc axit:
-
Muối trung hòa: Là muối mà trong gốc axit không còn nguyên tử hydro có thể thay thế bằng các nguyên tử kim loại.
Ví dụ: Na2SO4, CaCO3, KCl.
-
Muối axit: Là muối mà trong gốc axit vẫn còn nguyên tử hydro (H) chưa được thay thế bằng nguyên tử kim loại. Hóa trị của gốc axit bằng số nguyên tử hydro đã được thay thế bằng các nguyên tử kim loại.
Ví dụ: NaHSO4, NaHS, NaHCO3.
4. Sơ Đồ Tư Duy Axit Bazơ Muối: Mối Quan Hệ và Tổng Quan
Sơ đồ tư duy là công cụ hữu ích để hệ thống hóa kiến thức và nắm bắt mối liên hệ giữa các khái niệm. Dưới đây là sơ đồ tư duy tổng quan về axit, bazơ và muối:
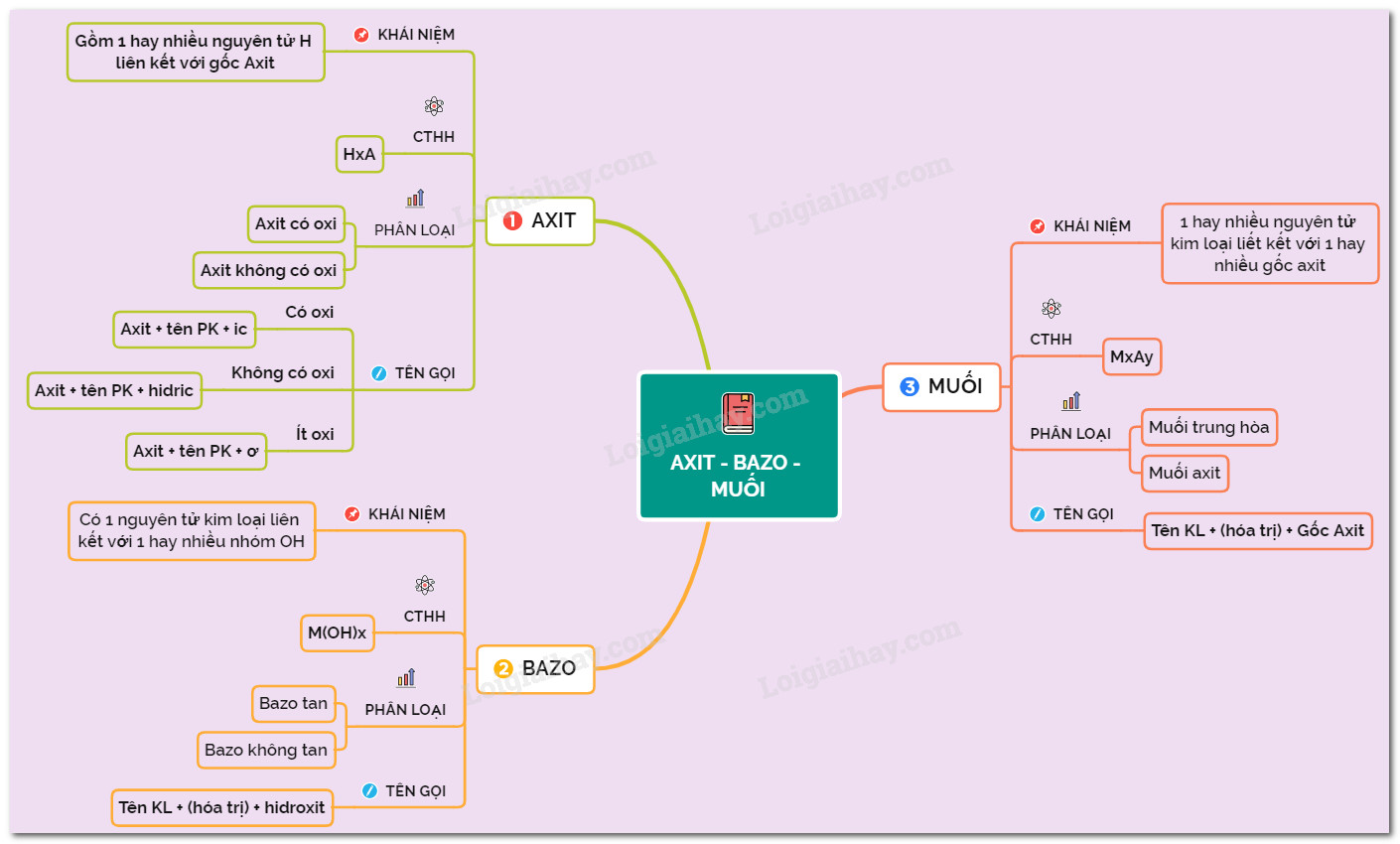 Sơ đồ tư duy tổng quan về axit, bazơ và muối, thể hiện mối quan hệ và tính chất cơ bản của chúng.
Sơ đồ tư duy tổng quan về axit, bazơ và muối, thể hiện mối quan hệ và tính chất cơ bản của chúng.
Sơ đồ này giúp chúng ta hình dung rõ ràng về định nghĩa, phân loại và cách gọi tên của axit, bazơ và muối, cũng như mối liên hệ giữa chúng trong các phản ứng hóa học.
5. Ứng Dụng Thực Tế của Axit, Bazơ và Muối
Axit, bazơ và muối không chỉ là những khái niệm lý thuyết mà còn có ứng dụng rộng rãi trong nhiều lĩnh vực của đời sống và công nghiệp:
- Trong công nghiệp: Axit sunfuric (H2SO4) được sử dụng rộng rãi trong sản xuất phân bón, chất tẩy rửa, và nhiều hóa chất khác. Bazơ như natri hidroxit (NaOH) được dùng trong sản xuất xà phòng, giấy và xử lý nước. Muối ăn (NaCl) là nguyên liệu quan trọng trong ngành công nghiệp thực phẩm và hóa chất.
- Trong nông nghiệp: Phân bón chứa các muối như amoni nitrat (NH4NO3) cung cấp dinh dưỡng cho cây trồng. Vôi (Ca(OH)2) được sử dụng để cải tạo đất chua.
- Trong y học: Axit clohidric (HCl) có trong dịch vị dạ dày giúp tiêu hóa thức ăn. Nhiều loại thuốc chứa các muối như natri bicacbonat (NaHCO3) để điều trị các bệnh liên quan đến tiêu hóa.
- Trong đời sống hàng ngày: Axit axetic (CH3COOH) có trong giấm ăn. Nước rửa chén thường chứa các bazơ để làm sạch dầu mỡ. Muối ăn (NaCl) là gia vị không thể thiếu trong nấu ăn.
Hiểu rõ về axit, bazơ và muối là nền tảng quan trọng để nắm vững kiến thức hóa học và ứng dụng chúng vào thực tế. Việc sử dụng sơ đồ tư duy giúp hệ thống hóa kiến thức một cách hiệu quả và dễ dàng ghi nhớ.

