Phản ứng giữa nhôm (Al) và dung dịch natri hidroxit (NaOH) là một phản ứng hóa học quan trọng trong chương trình hóa học phổ thông. Phản ứng này tạo ra khí hidro (H2) và dung dịch natri aluminat (NaAlO2). Dưới đây là phân tích chi tiết về phản ứng này, đặc biệt khi cho 2.7 gam Al tác dụng hoàn toàn với dung dịch NaOH dư.
Phương trình hóa học của phản ứng:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
Từ phương trình trên, ta thấy rằng 2 mol Al sẽ tạo ra 3 mol H2.
Để tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn (đktc), ta cần xác định số mol của Al.
Số mol của Al được tính như sau:
nAl = mAl / MAl
Trong đó:
- mAl là khối lượng của Al (2.7 gam)
- MAl là khối lượng mol của Al (27 g/mol)
nAl = 2.7 / 27 = 0.1 mol
Theo phương trình phản ứng, tỉ lệ mol giữa Al và H2 là 2:3. Vậy số mol H2 tạo ra là:
nH2 = (3/2) nAl = (3/2) 0.1 = 0.15 mol
Thể tích khí H2 ở điều kiện tiêu chuẩn (đktc) được tính bằng công thức:
VH2 = nH2 * 22.4
Trong đó:
- nH2 là số mol của H2 (0.15 mol)
- 22.4 là thể tích mol của khí ở đktc (lít/mol)
VH2 = 0.15 * 22.4 = 3.36 lít
Vậy, khi cho 2.7 gam Al tác dụng hoàn toàn với dung dịch NaOH dư, thể tích khí H2 thu được ở điều kiện tiêu chuẩn là 3.36 lít.
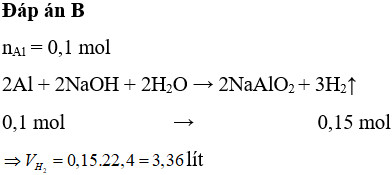 Phản ứng Al với NaOH tạo khí hidro
Phản ứng Al với NaOH tạo khí hidro
Sơ đồ phản ứng nhôm tác dụng với natri hidroxit (NaOH) tạo thành khí hidro (H2) và natri aluminat (NaAlO2).
Các yếu tố ảnh hưởng đến tốc độ phản ứng:
Một số yếu tố có thể ảnh hưởng đến tốc độ phản ứng giữa Al và NaOH, bao gồm:
- Nồng độ NaOH: Nồng độ NaOH càng cao, tốc độ phản ứng càng nhanh.
- Nhiệt độ: Nhiệt độ tăng, tốc độ phản ứng tăng.
- Kích thước hạt Al: Al ở dạng bột mịn sẽ phản ứng nhanh hơn so với Al ở dạng khối lớn do diện tích tiếp xúc lớn hơn.
- Khuấy trộn: Khuấy trộn giúp tăng cường sự tiếp xúc giữa Al và NaOH, làm tăng tốc độ phản ứng.
Ứng dụng của phản ứng:
Phản ứng giữa Al và NaOH có nhiều ứng dụng trong thực tế, bao gồm:
- Sản xuất khí H2 trong phòng thí nghiệm: Phản ứng này là một phương pháp đơn giản để điều chế khí H2.
- Khắc etching bề mặt kim loại: Dung dịch NaOH có thể được sử dụng để khắc các hoa văn, họa tiết trên bề mặt nhôm.
- Sản xuất natri aluminat: NaAlO2 là một hợp chất quan trọng được sử dụng trong xử lý nước và sản xuất giấy.
Lưu ý khi thực hiện phản ứng:
Khi thực hiện phản ứng giữa Al và NaOH, cần lưu ý một số điểm sau:
- Sử dụng đồ bảo hộ: NaOH là một chất ăn mòn, cần sử dụng găng tay, kính bảo hộ để tránh tiếp xúc trực tiếp với da và mắt.
- Thực hiện trong tủ hút: Phản ứng tạo ra khí H2, có thể gây nổ nếu tích tụ trong không gian kín.
- Kiểm soát tốc độ phản ứng: Phản ứng có thể diễn ra rất nhanh, cần kiểm soát lượng Al và NaOH để tránh phản ứng quá mạnh.
Hiểu rõ về phản ứng “Cho 2 7 Gam Al Tác Dụng Hoàn Toàn Với Dung Dịch Naoh Dư” giúp học sinh nắm vững kiến thức hóa học và áp dụng vào giải các bài tập liên quan.


